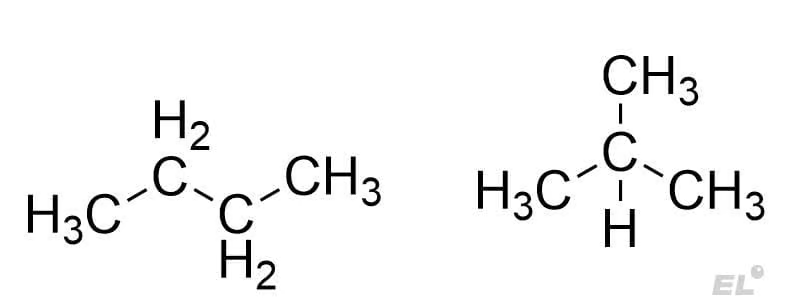Алканы
963
Любой курс органической химии начинается с алканов. Для алканов характерны:
- Наличие только одинарных связей углерод – углерод, поэтому алканы являются предельными углеводородами или насыщенными соединениями;
- Низкая реакционная способность, для них характерны реакции, идущие по радикальному механизму;
- Все углероды в алканах sp3-гибридизованы.
Любой алкан CnH2n+2 можно так же написать в виде RH, где R = CnH2n+1 (радикал, алкильный заместитель). Представители низших (по количеству атомов углерода) алканов и соответствующих алкильных фрагментов представлены в таблице.
| Алкан RH | Название алкана RH | Название радикала R |
| CH4 | метан | метил CH3— |
| C2H6 | этан | этил CH3CH2— |
| CH3CH2CH3 | пропан | пропил CH3CH2CH2— |
| CH3CH2CH2CH3 | бутан | н-бутил CH3CH2CH2CH2— |
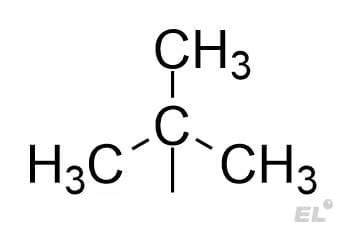 | изобутан | изобутил |
Как видно, первые три по счёту алканов не имеют изомеров, для алканов, начиная с четвёртого (бутана) характерна структурная изомерия. Так же для некоторых алканов характерна оптическая изомерия.
Основные химические свойства алканов
- Как и любые органические вещества, алканы могут сгорать в избытке кислорода O2. Например, горение этана в кислороде:
2C2H6 + 7O2 → 4CO2 + 6H2O
- Для алканов характерны реакции радикального замещения.
Этот тип реакций наиболее характерный и распространённый для алканов. Радикальное галогенирование (например, с хлором и бромом) идёт по следующей схеме:
RH + Cl2 → RCl + HCl
RH + Br2 → RBr + HBr
В качестве условий этой реакции выступает электромагнитное излучение: свет в видимом или ультрафиолетовом частотном диапазоне (над стрелкой можно написать 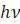 или свет, но на ЕГЭ это не обязательно). Также для алканов характерна реакция нитрования (реакция Коновалова) с разбавленной азотной кислотой при нагревании:
или свет, но на ЕГЭ это не обязательно). Также для алканов характерна реакция нитрования (реакция Коновалова) с разбавленной азотной кислотой при нагревании:
RH + HNO3 → RNO2 + H2O
Несмотря на кажущуюся простоту в этих реакциях есть подводные камни. Проблемы начинаются, когда рассматриваются разветвлённые алканы по типу изобутана. Попробуем бромировать и нитровать изобутан:
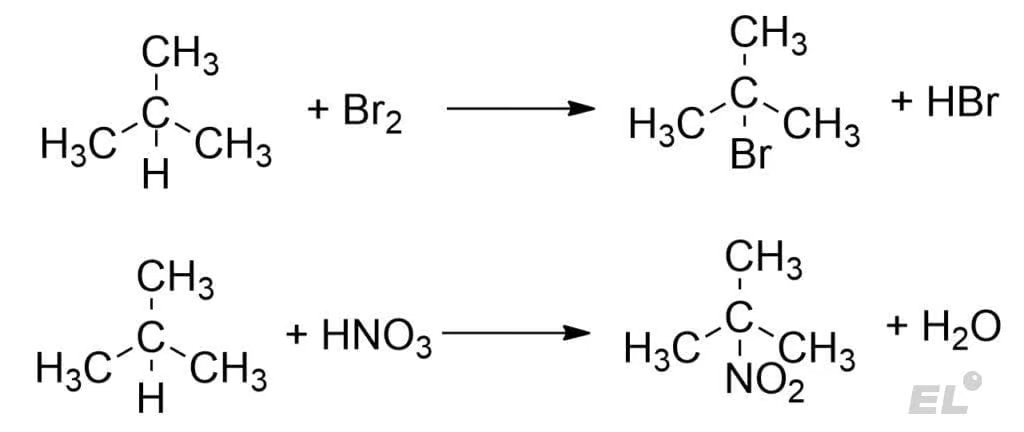
В обеих реакциях написан доминирующий продукт: галогенирование и нитрование пройдёт у третичного атома углерода, а не у первичного атома углерода. То есть, в таких реакциях следует соблюдать правило, что преимущественно замещение водорода на галоген и нитрогруппу произойдёт в порядке третичный атом углерода > вторичный атом углерода > первичный атом углерода.
- Термическое разложение метана.
Оно может протекать в двух вариациях. В первом варианте, реализирующихся при температурах порядка 10000C, метан разлагается на углерод и водород:
CH4 → C + 2H2
Во втором варианте, температура достигает порядка 15000C, и метан разлагается на ацетилен и водород:
2CH4 → C2H2 + 3H2
- Дегидрирование, дегидроциклизация и дегидроароматизация алканов.
Дегидрирование представляет собой реакцию отщепления водорода H2. Эту реакцию обычно катализируют металлы типа Pt или Ni (реакция идёт при нагревании), например, дегидрирование этана в этилен:
C2H6 → CH2=CH2 + H2
Для алканов типа пентана и гексана возможны реакции дегидрирования, сопровождающиеся замыканием углеводородной цепочки в цикл. Например, дегидроциклизация гексана в циклогексан и дегидроароматизация гексана в бензол:
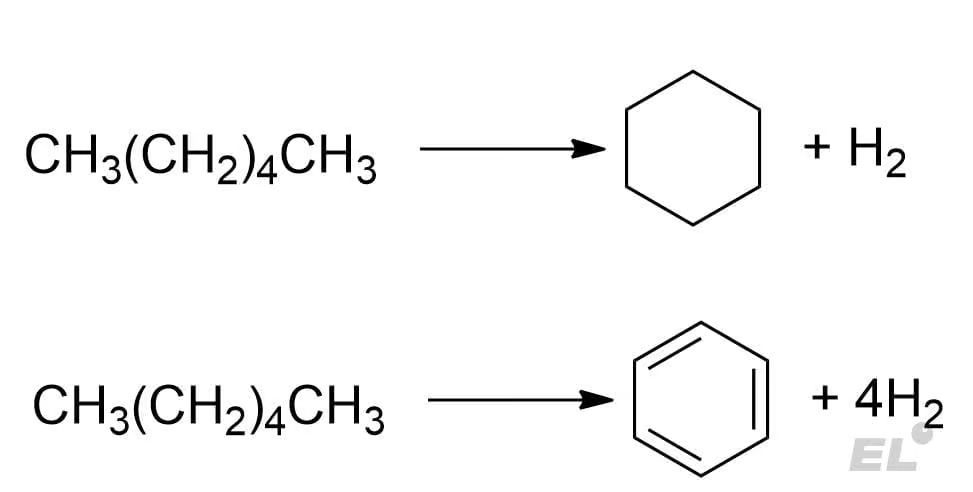
Способы получения алканов
- Реакция Вюрца.
Реакция формально протекает по очень простой схеме, берётся алкилгалогенид и проводится его реакция с металлическим натрием:
2RCl + 2Na → R-R + 2NaCl
2RBr+ 2Na → R-R + 2NaBr
2RI + 2Na → R-R + 2NaI
Пример такой реакции:
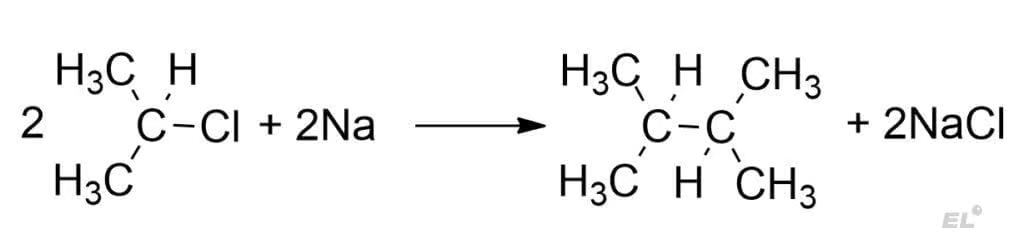
Важно: идёт образование связи между теми углеродами, при которых находился атом галогена.
- Электролиз солей карбоновых кислот (реакция Кольбе).
Электролиз растворов солей карбоновых кислот позволяет легко получать симметричные алканы типа R-R по следующей реакции:
2RCOONa + 2H2O → R-R + 2CO2 + H2 + 2NaOH
На катоде происходит выделение водорода H2, на аноде выделяется углекислый газ CO2 и образуется алкан R-R.
- Реакция Дюма.
Тут тоже пригодятся соли карбоновых кислот, однако берётся соль карбоновой кислоты в твёрдом виде и сплавляется с твёрдой щёлочью:
RCOOK + KOH → RH + K2CO3
- Гидролиз метанида алюминия.
Гидролиз карбида алюминия – простой способ получения газообразного метана:
Al4C3 + 12H2O → 3CH4 + 4Al(OH)3
Можно проводить эту реакцию в кислой и щёлочной средах:
Al4C3 + 12HCl → 3CH4 + 4AlCl3
Al4C3 + 4NaOH + 12H2O → 4Na[Al(OH)4] + 3CH4
Блок-схема методов получения алканов.
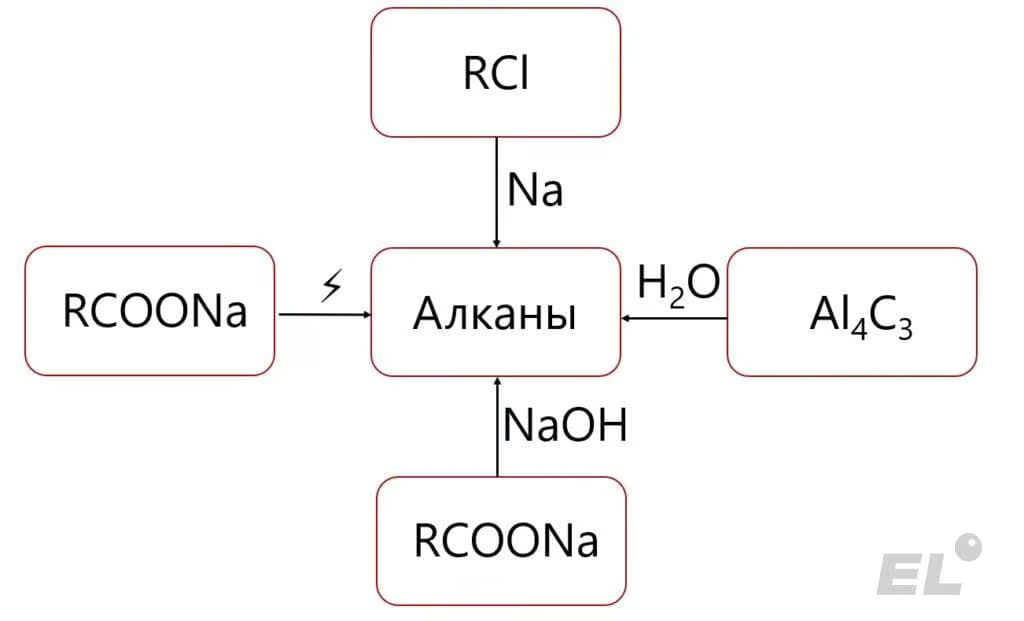
Резюме:
- Алканы – класс предельных углеводородов с общей формулой CnH2n+2, в котором все атомы углерода связаны между собой одинарными связями и sp3-гибридизованы;
- Для алканов характерна структурная и оптическая изомерия;
- Алканы вступают в реакции радикального замещения с галогенами и азотной кислотой;
- Основные способы получения алканов: реакции Вюрца, Дюма и Кольбе, а также гидролиз (в различных средах) карбида алюминия.
Примеры задач на эту тему:
Задание 1. Задача №11 (тестовая часть)
Из предложенного перечня выберите два вещества, в молекулах которых все атомы углерода находятся в sp3-гибридном состоянии.
- бензол;
- н-бутан;
- пропен;
- бутадиен-1,3; 5) изобутан.
25
Задание 2. Задача № 14 (тестовая часть)
Установите соответствие между исходными веществами и продуктами, которые преимущественно образуются при их взаимодействии с бромом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
НАЗВАНИЕ ВЕЩЕСТВА ПРОДУКТ
А) этан 1) CH3Br
Б) н-бутан 2) CH3CH2CH2Br
В) метан 3) CH3CHBrCH3
Г) пропан 4) CH3CH2Br
5) CH3CH2CH2CH2Br
6) CH3CHBrCH2CH3
4613
Задание 3. Задача № 32 (вторая часть)
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
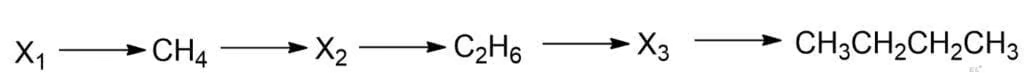
- CH3COONa + NaOH → CH4 + Na2CO3
- CH4 + Br2 → CH3Br + HBr
- 2CH3Br + 2Na → C2H6 + 2NaBr
- CH3CH3 + Cl2 → CH3CH2Cl + HCl
- 2CH3CH2Cl + 2Na → CH3CH2CH2CH3 + 2NaCl
Определения:
- Алканы – класс органических соединений (если точнее, то углеводородов, так как содержатся только атомы углерода и водорода) с общей формулой CnH2n+2, где n = 1,2,3,…
- Предельный углеводород (насыщенный углеводород) – любой углеводород, в котором нет двойных и тройных связей между углеродами, то есть имеются только одинарные связи между углеродами.
- Радикальный механизм – механизм, включающий в себя стадии образования высокореакционных частиц с одним или более неспаренным электроном – радикалов.
- sp3-гибридизованный углерод – такой атом углерода, который образует 4 одинарных связи.
- Изомеры – вещества, обладающие одной и той же молекулярной формулой, но различающиеся положением атомов друг относительно друга в молекуле (различаются структурной формулой). Изомеры отличаются по своим физико-химическим свойствам, то есть разные изомеры одного и того же вещества, например, могут иметь разные температуры кипения, плавления, разные показатели преломления и вступать в реакции по-разному.
- Структурная изомерия – вид изомерии, заключающийся в различном строении углеводородного скелета (различном положении атомов углерода друг относительно друга). Характерный пример такой изомерии это пара бутана нормального строения (н-бутан) и изобутана:

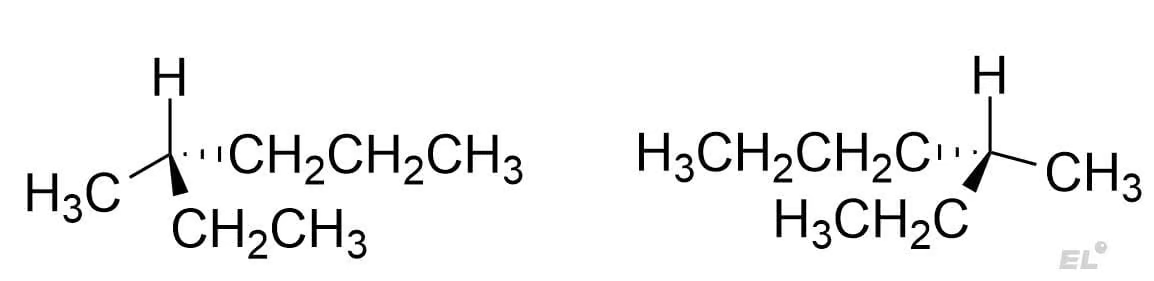
- Оптическая изомерия – данная изомерия проявляется для молекул, содержащих углерод, окружённый четырьмя различными заместителями (такой углерод называют хиральным). Для таких молекул их зеркальное отражение не может быть совмещено с исходной молекулой. Пример:

- При желании про электромагнитное излучение можно вставить отдельную мини статью, это особо никогда не делается в курсах химии, но будет интересно.
Разберёмся что такое свет. Для этого возьмём какую-нибудь систему отсчёта: систему координат Oxyz и часы, которые будут нам отсчитывать время t. Пусть электрическое поле (зелёный вектор) направлено по оси x, магнитное поле (синий вектор) направлено по оси y, а вдоль красного вектора (по оси z) электрическое и магнитное поле бегут (распространяются). Эта конструкция и есть электромагнитная волна! У нас в каждой точке нашего мира, в котором мы живём со временем распространяются два этих векторочка (синий и зелёный) — это и есть электромагнитная волна (или одна частица света — фотон!). Свет — это бесконечный набор самых разных таких электромагнитных волн (фотонов), которые различаются как длиной этих трёх (красного, зелёного и синего) векторов, так и их направлением.
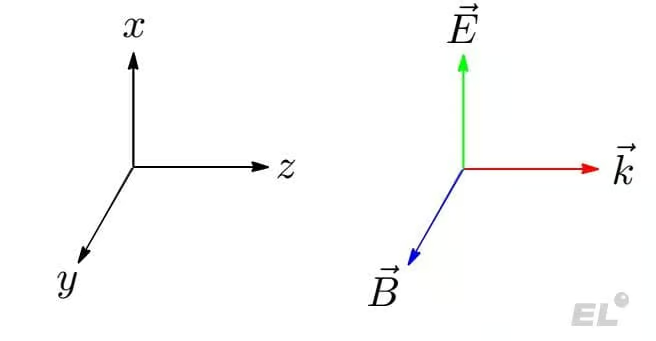
Теперь как нам оно пригодится в химии? Зелёный и синий векторочек в каждой точке нашего мира со временем меняют свою длину (и, возможно, направление), то есть колеблются, что позволяет приводить в движение электроны химических связей, в ходе такого своеобразного танца электронов под действием колеблющихся зелёного и синего векторочков химическая связь рвётся!
Разберёмся как это описать количественно. Возьмём для примера зелёный векторочек (вектор электрического поля), он направлен вдоль оси x и бежит вдоль оси z, как было сказано, он любит колебаться, поэтому он в каждой точечке нашего мира имеет разную длину и может быть направлен как по оси x, так и против неё. Однако мы можем выделить своеобразный период — кратчайшее расстояние между двумя самыми длинными или короткими (когда зелёный векторочек нулевой вектор — зелёная точка) зелёными векторами — это величина и есть длина волны (лямбда, фиолетовая дуга).
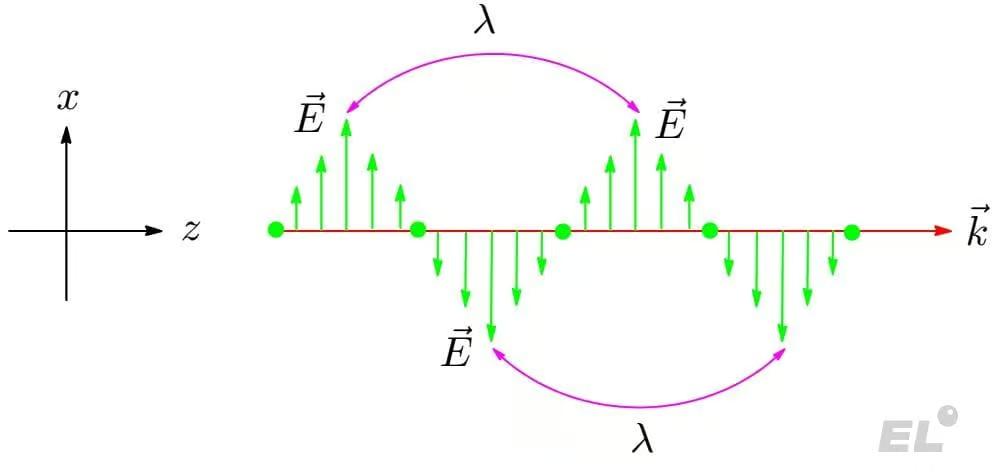
Каждая такая электромагнитная волна (каждый фотон) несёт определённую энергию, которая и тратится на разрыв связи. Тогда, если мы захотим разорвать 1 моль связей (6,02·1023 штук связей), то нам надо направить на нашу связь 1 моль таких электромагнитных волн, тогда по закону сохранения энергии мы можем написать:
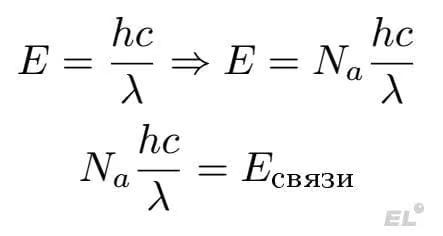
где h = 6,63·10-34 Дж·с (постоянная Планка), c = 3·108 м/с (скорость света в вакууме)
Тогда если мы хотим порвать, например, связи Cl-Cl (240 кДж/моль связей) и Br-Br (190 кДж/моль), то по формуле получаем около 500 нм для Cl2 (наши рецепторы в глазу фиксируют такие электромагнитные волны как зелёный цвет, точнее зелёный и синий векторочек колеблют электроны в молекулах наших глазных рецепторов и мы это ощущаем как зелёную картинку) и 630 нм для Br2 (оранжево-красный цвет), поэтому если мы хотим хлорировать и бромировать, например, метан:
CH4 + Cl2 → CH3Cl + HCl
CH4 + Br2 → CH3Br + HBr
то нам подойдёт свет с длиной волны в первой реакции меньше 500 нм (это и видимый глазами свет, и ультрафиолет 100-200 нм), а во второй меньше 630 нм (это и видимый свет, и ультрафиолет 100-200 нм.
- Третичный атом углерода – атом углерода, связанный с тремя углеродами.
- Вторичный атом углерода – атом углерода, связанный с двумя углеродами.
- Первичный атом углерода – атом углерода, связанный с одним углеродом.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND