Гидролиз
1044
Задумывались ли вы, что происходит с твёрдой солью, когда вы её растворяется в воде? Давайте ответим на этот вопрос:
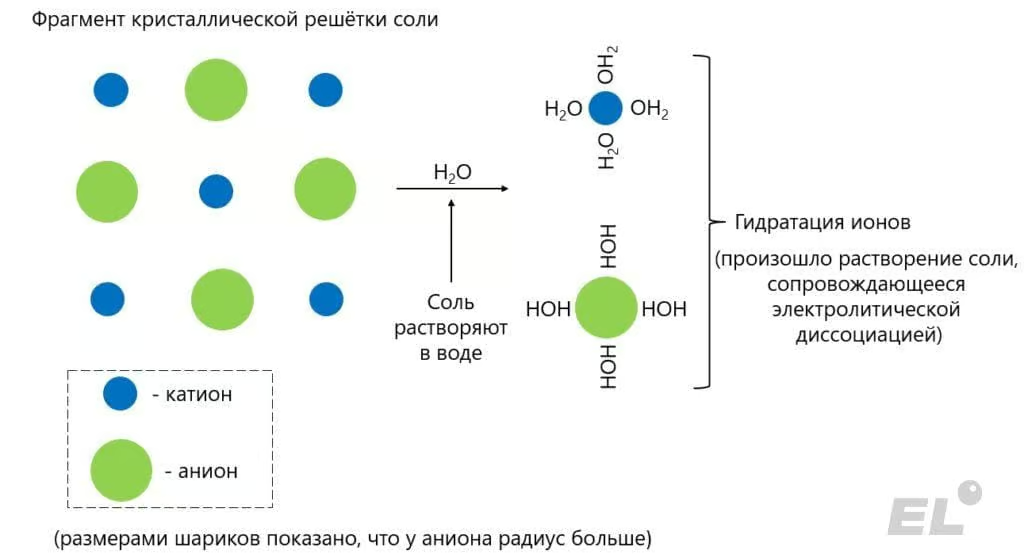
У соли ионная решётка – в узлах решётки располагаются катионы и анионы. Вода сама по себе полярная молекула – на одном её конце сосредоточен отрицательный заряд, а на другом её конце – водородах – уже положительный заряд, поэтому вода может прекрасно взаимодействовать с ионами. К чему это ведёт? Вода прямо-таки разрушает ионную решётку соли, давая отдельные катионы и анионы, из которых состоит решётка соли. Причём эти ионы покрыты гидратной шубой, которая очень выгодная и компенсирует затраты энергии, которые пошли на разрушение решётки. Обычно это всё записывается как реакция электролитической диссоциации соли:
NaCl = Na+ + Cl—
Zn(NO3)2 = Zn2+ + 2NO3—
А что происходит дальше? Катионы и анионы могут вступать в химическую реакцию с молекулами воды, но какое условие для этой реакции? Давайте, возьмём хлорид натрия, возможны следующие реакции:
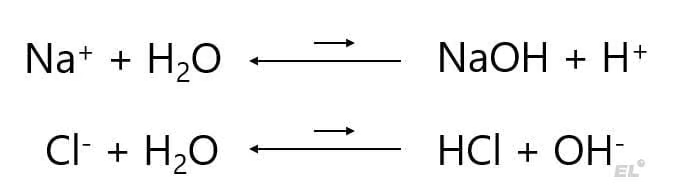
Однако в виду того, что гидроксид натрия и соляная кислота – сильные электролиты – равновесие практически полностью смещено в сторону исходные веществ, то есть ионы не реагируют с водой, или, что то же самое, не подвергаются гидролизу.
Изменим ситуацию и заменим NaCl на NaF:
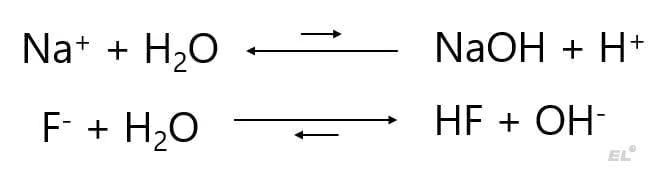
Ситуация изменилась: HF – кислота слабая, поэтому фторид-анион подвергается гидролизу и в растворе появляется избыток гидроксид-ионов OH—. Можем сформулировать интересное правило:
- Гидролизу подвергается катион/анион, соответствующий слабому основанию/кислоте.
Среда раствора
В прошлом примере мы увидели, что при помещении твёрдого NaF в воду, происходит разрушение кристаллической решётки соли, гидратация ионов, а затем фторид-ион ещё может реагировать с водой, давая избыток анионов OH— в растворе. Как мы можем количественно описывать количественное соотношение между ионами H+ и OH— в растворе, ну, вообще, принципиально возможны 3 ситуации:
- Концентрация ионов H+ превышает концентрацию OH— — такую среду называют кислой;
- Концентрация ионов H+ равна концентрации ионов OH— — такая среда называется нейтральной;
- Концентрация ионов OH— превышает концентрацию H+ — щелочная среда.
Речь идёт именно о молярной концентрации. Для того, чтобы удобно классифицировать (количественно) среду вопроса ввели водородный показатель pH, который представляет собой десятичный логарифм от концентрации ионов водорода в растворе, взятый с обратным знаком:
pH = -lg[H+]
Где lg – логарифм по основанию 10, [H+] – концентрация ионов водорода, теперь становится понятным обозначение pH:
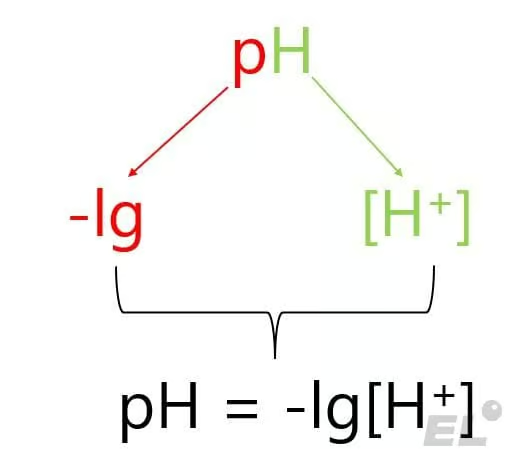
Запоминать связь pH с средой раствора не придётся, для этого на ЕГЭ даются следующие справочные данные (это всё актуально для температуры 25 градусов Цельсия и давления 1 атмосфера):

Ну всё, в целом, мы готовы утвердить общее правило определения среды раствора:
- Среда раствора определяется гидролизом катиона/аниона, который соответствует слабому основанию/кислоте;
- Причём если гидролизу подвергается катион – такой процесс называется гидролизом по катиону;
- Если гидролизу подвергается анион – такой процесс называется гидролизом по аниону.
Разберём типовые примеры определения среды растворов солей, кислот и щёлочей.
| Вещество | Комментарий | Среда раствора |
| NaCl | Не подвергается гидролизу | Нейтральная |
| NaF | Гидролиз по аниону | Слабо щёлочная |
| Zn(NO3)2 | Гидролиз по катиону | Слабо кислая |
| H2SO4 | Сильная кислота | Сильно кислая |
| NaOH | Сильное основание (щёлочь) | Сильно щёлочная |
| NaHCO3 | Гидролиз по аниону | Слабо щёлочная |
| NaHSO4 | Серная кислота – сильная, поэтому кислотный остаток диссоциирует HSO4— = H+ + SO42- | Слабо кислая |
| Al2S3 | Гидролиз и по катиону, и по аниону (совместный гидролиз) | Произойдёт реакция полного необратимого гидролиза: Al2S3 + 6H2O = 2Al(OH)3 + 3H2S |
Как же визуально определять какая среда у раствора? Очень просто – поместить в него вещество, которое меняет свою окраску в зависимости от среды раствора – такие вещества называются индикаторами:
| Индикатор | Окраска индикатора в кислой среде | Окраска индикатора в нейтральной среде | Окраска индикатора в кислой среде |
| Фенолфталеин | бесцветный | бесцветный | малиновый |
| Метилоранж | красный | оранжевый | жёлтый |
| Лакмус | красный | фиолетовый | синий |
Резюме
- При помещении твёрдой соли в воду – она подвергается растворению и электролитической диссоциации;
- Гидратированные катионы и анионы могут вступать в реакцию с водой;
- Катион/анион, соответствующий слабому основанию/кислоте, подвергаются гидролизу;
- Среда раствора определяется водородным показателем pH.
Примеры задач на эту тему:
Задание 1. Задача №21 (из тестовой части)
Расположите водные растворы веществ, обладающие одинаковой молярной концентрацией, по возрастанию значения pH их водных растворов:
- AlCl3
- NaHCO3
- H2SO4
- NaOH
3124
Задание 2. Задача №21 (из тестовой части)
Расположите водные растворы веществ, обладающие одинаковой молярной концентрацией, по убыванию значения pH их водных растворов:
- NaHSO4
- KCl
- KF
- HNO3
3214
Задание 3. Задача №31 (из открытой части)
Гидроксид алюминия растворили в соляной кислоте. К полученному раствору прилили раствор гидрокарбоната натрия, при этом одновременно выпал белый и осадок и выделился газ. Газ поглотили минимально возможным количеством щёлочи, а осадок растворили в щёлочи. Напишите уравнения четырёх описанных реакций:
- Al(OH)3 + 3HCl = AlCl3 + 3H2O
- AlCl3 + 3NaHCO3 = Al(OH)3 + 3CO2 + 3NaCl
- NaOH + CO2 = NaHCO3
- Al(OH)3 + NaOH = Na[Al(OH)4]
Определения:
- Гидролиз – реакция между водой и растворёнными в ней ионами после электролитической диссоциации.
- Молярная концентрация C (в моль/л) суть отношение количества растворённого вещества (в моль) n к объёму раствора (в л) V: C = n/V.
- Логарифм logba от какого-либо числа a (или функции) по основанию b, это такое число c, что возведение b в степень c даёт искомое число a: bc = a или logba = c.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND










