Металлы IA группы
1064
Металлы первой группы главной подгруппы – это щелочные металлы:
- Литий Li;
- Натрий Na;
- Калий K;
- Рубидий Rb;
- Цезий Cs;
- Франций Fr – также известный как «сладкая булочка», так как обладает наименьшей электроотрицательностью.
Важные свойства щелочных металлов:
- Они все имеет конфигурацию валентного слоя ns1, поэтому имеют две характерные степени окисления 0 и +1;
- Щелочные металлы имеют высокую восстановительную активность так как очень хотят кому-нибудь отдать свой электрон с ns1 и получить конфигурацию ns0, становясь катионами;
- Такая высокая восстановительная активность обуславливает, как правило, высокую экзотермичность многих реакций с их участием, например щелочные металлы реагируют с водой со взрывом – из-за чего их приходится хранить под слоем органических растворителей (например, керосина);
- Соли щелочных металлов, помещённые в пламя горелки, окрашивают пламя в определённый цвет: для солей лития малиновая окраска, натрия – жёлтая, калия – фиолетовая, рубидия – тёмного красная, цезия — голубая.
Рассмотрим как формируется цвет пламени при внесении в него различных солей на примере сульфата меди (для солей других металлов это работает аналогично). Высокая температура в пламени горелки даёт очень много теплоты (тепловой энергии), которая идёт на разрушение ионной решётки сульфата меди. Часть сульфата меди атомизуется и в пламени появляется немного атомов меди. Эти атомы меди и придают пламени зелёную окраску. Каким образом появляется эта зелёная окраска? Валентные электроны в атоме меди в основном электронном состоянии образуют конфигурацию 3d10 4s1, при нагревании тепловая энергия передаётся электронам – и происходит переход атома меди в возбуждённое состояние: для простоты пусть это будет конфигурация 3d9 4s2. Естественно, атомам меди невыгодно быть в такой конфигурации и они хотят вернуться назад, электроны возвращаются в исходную конфигурацию 3d10 4s1, а избыточная энергия при этом выделяется в виде зелёного света, который мы и видим в виде зелёных языков пламени.
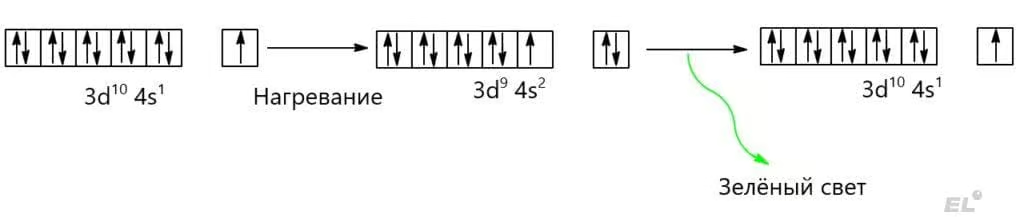
Атомы меди переходят из основного состояния в возбуждённое за счёт тепловой энергии, затем возвращаются в основное состояние, выделяя избыточную энергию в виде зелёного света.
Окрашивание пламени в какой-либо цвет, скажем, щелочными металлами, работает ровно так же. Природа металла определяет цвет пламени, который будет зафиксирован нашими рецепторами в глазу.
Способы получения щелочных металлов
Поскольку щелочные металлы – очень активные, то их можно получить электролизом именно расплава соответствующих солей:
2NaCl (расплав) = 2Na + Cl2
В то же время, в случае электролиза соответствующих растворов вместо осаждённого металла будет выделяться газообразный водород на катоде.
Химические свойства щелочных металлов
- Реакции с неметаллами
Щелочные металлы прекрасно реагируют с неметаллами за счёт своего хорошего восстановительного потенциала. Например, натрий в реакции с водородом легко даёт гидрид натрия:
2Na + H2 = 2NaH
Литий реагирует с азотом, давая нитрид лития:
6Li + N2 = 2Li3N
По-особому идут реакции с неметаллами, литий с кислородом даёт оксид:
4Li + O2 = 2Li2O
Натрий даёт уже пероксид:
2Na + O2 = Na2O2
А калий и оставшиеся щелочные металлы – надпероксиды:
K + O2 = KO2
Приведём в этом же разделе характерные особенности пероксидов.
| Свойство | Пример |
| Высокая окислительная способность | Na2O2 + SO2 → Na2SO4 |
| Восстановительная активность (с более сильными окислителями) | 5Na2O2 + 2KMnO4 + 8H2SO4 → 5O2 + 2MnSO4 + 5Na2SO4 + K2SO4 + 8H2O |
| Реакция с водой (или кислотами) при разных условиях | С водой при охлаждении реакция протекает без изменения степени окисления: Na2O2 + H2O = 2NaOH + H2O2 При нагревании перекись водорода разлагается на воду и кислород: 2Na2O2 + 2H2O = 4NaOH + O2 (окислительно-восстановительная реакция) |
- Реакции с водой, солями и кислотами
Щелочные металлы как активные металлы могут замещать менее активные металлы из солей, вытеснять водород из кислот и окисляться кислотами-окислителями типа азотной и концентрированной серной. Однако во всех этих реакциях есть одно затруднение, щелочные металлы будут преимущественно реагировать в начале с водой (реакция идёт с выделением большого количества теплоты и со взрывом):
2Li + 2H2O = 2LiOH + H2
Кстати, в ходе этой реакции образовалась щёлочь LiOH, перейдём к химическим свойствам щёлочей.
Химические свойства щёлочей
Щёлочи – в первую очередь основные гидроксиды, поэтому они готовы реагировать со всем кислотным (или тем, что проявляет кислотные свойства), то есть с кислотными оксидами, кислотами, амфотерными оксидами и гидроксидами:
2NaOH + H2SO4 = Na2SO4 + 2H2O
NaOH + H2SO4 (избыток) = NaHSO4 + H2O
2NaOH + CO2 = Na2CO3 + H2O
KOH + Al(OH)3 = K[Al(OH)4]
Ровно эти же свойства справедливы и для оксидов щелочных металлов (основных оксидов). Также щёлочи могут реагировать с солями аммония, выделяя аммиак:
NH4Cl + KOH = KCl + NH3 + H2O
Это пример реакции ионного обмена, другие примеры:
2AgNO3 + 2NaOH = Ag2O (чёрный осадок) + 2NaNO3 + H2O
(в ходе этой реакции распадается неустойчивый гидроксид серебра(I))
NaH2PO4 + 2NaOH (избыток) = Na3PO4 + 2H2O
NaH2PO4 + NaOH = Na2HPO4 + H2O
Интересны реакции амфотерных металлов с щёлочью:
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2
Кремний окисляется щёлочами, а галогены, сера и фосфор в них диспропорционируют:
| Реакция | Комментарий |
| Si + 2NaOH + H2O = Na2SiO3 + 2H2 | В этой реакции окислителем является H+1 |
| 2KOH + Cl2 (любой галоген, кроме фтора) = KClO + KCl + H2O | Идёт при охлаждении |
| 6NaOH + 3Cl2 (любой галоген, кроме фтора) = NaClO3 + 5NaCl + 3H2O | Идёт при нагревании |
| 4S + 8NaOH = 3Na2S + Na2SO3 + 4H2O | В избытке серы возможно образование тиосульфата Na2S2O3 |
| 4P + 3KOH + 3H2O = PH3 + 3KH2PO2 | Вместо 4P можно писать P4 (белый фосфор) |
Резюме:
- Металлы первой группы главной подгруппы – щелочные металлы, для них характерные степени окисления 0, +1;
- Щелочные металлы обладают большой восстановительной способностью;
- Для гидроксидов и оксидов щелочных металлов характерны основные свойства.
Примеры задач на эту тему:
Задание 1. Задача №9 (тестовая часть)
Задана следующая цепочка превращений:
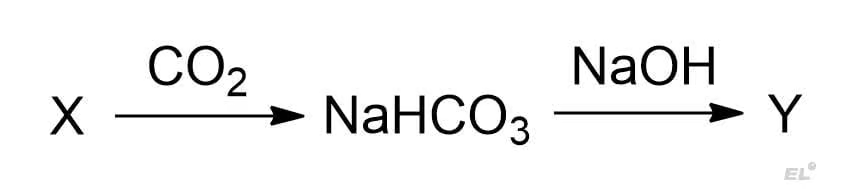
Определите, какие из указанных веществ являются веществами X и Y:
- соляная кислота
- гидроксид калия
- гидроксид натрия
- карбонат натрия
- поташ
Задание 2. Задача №31 (открытая часть)
Литий оставили в атмосфере азота. Полученный твёрдый остаток растворили в воде, наблюдая выделение двух разных по химической природе газов. Один из этих газов растворяется в соляной кислоте. Напишите уравнения четырёх описанных реакций.
Задание 3. Задача №31 (открытая часть)
Расплав хлорида натрия подвергли электролизу на инертных электродах. Полученное твёрдое вещество сожгли в кислороде, продукт данной реакции растворили в горячей воде, затем к образовавшемуся раствору прилили сульфат меди(II), наблюдая образование синего осадка.
Определения:
- Экзотермическая реакция – реакция, идущая с выделением теплоты.
- Оксид – бинарное кислород-содержащее вещество, где степень окисления кислорода составляет -2.
- Пероксид – бинарное кислород-содержащее вещество, где у кислорода степень окисления -1 и присутствует пероксидный мостик O-O.
- Надпероксид (супероксид) – бинарное кислород-содержащее вещество, содержащее в своём составе анион O2—.
- Щёлочь – растворимый в воде сильный основный гидроксид.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND










