Металлы IIA группы
1560
Во второй группе главной подгруппе нас ожидают:
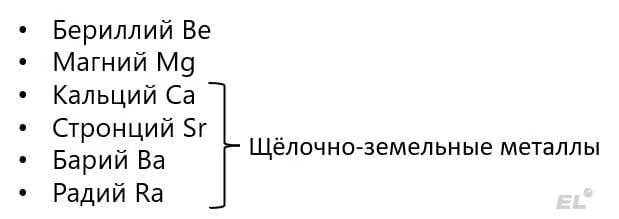
Такая неоднородность по сравнению с щелочными металлами легко осознаётся, если мы посмотрим на соответствующие гидроксиды:
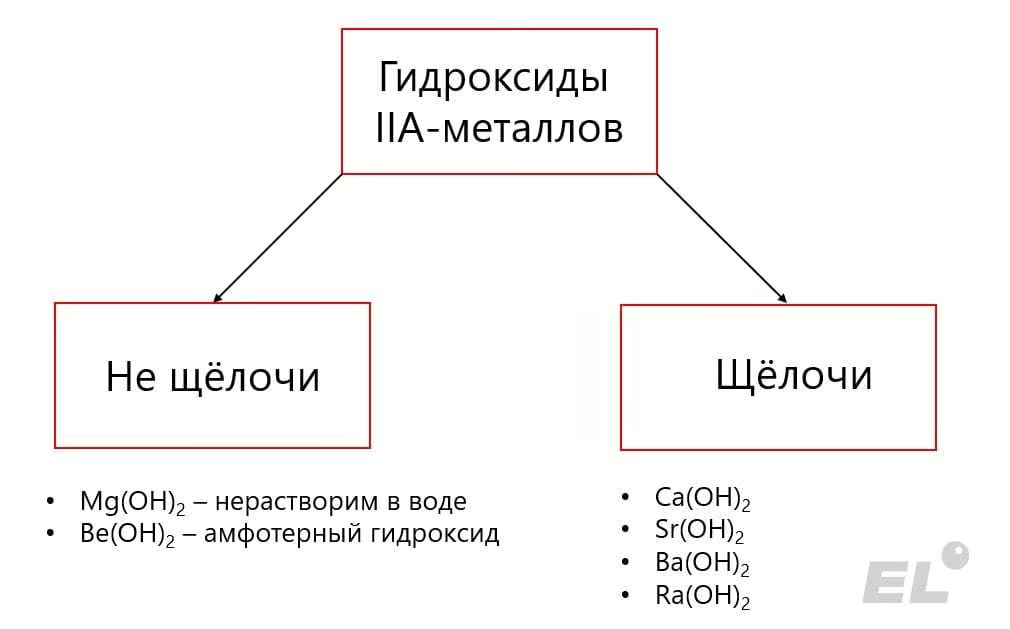
- Be(OH)2 – амфотерный гидроксид;
- Mg(OH)2 – основный гидроксид, нерастворимый в воде;
- Остальные металлы образуют щёлочи – щёлочно-земельные металлы.
Для всех этих металлов характерными степенями окисления являются 0 и +2, поскольку конфигурация внешнего слоя ns2.
Химические свойства металлов второй группы главной подгруппы
Металлы второй группы главной подгруппы всё ещё являются сильными восстановителями, но чуть менее сильными восстановителями по сравнению с щелочными металлами. Химические свойства данных металлов, в целом, весьма схожи с щелочными металлами. Так, например, магний растворяется в воде лишь при нагревании (с горячей водой):
Mg + 2H2O = Mg(OH)2 + H2
Щелочные металлы, напомним, реагируют с водой значительно активнее, давая взрыв. Другие примеры химических свойств приведены в таблице:
| Реакция | Комментарий |
| Ca + 2H2O → Ca(OH)2 + H2 | Растворение кальция в воде |
| Ca + H2SO4 (разб) → CaSO4 + H2 | Реакция с кислотами становится доступной в виду не такой большой активности металлов |
| 4Mg + 5H2SO4(конц) → 4MgSO4 + H2S + 4H2O | Магний активный металл, поэтому восстановление серной кислоты идёт до сероводорода |
| Mg + Zn(NO3)2 → Mg(NO3)2 + Zn | Вытеснение менее активного (в ряду напряжений) цинка |
| Ca + C2 → CaC2 | Образование карбида (ацетиленида) кальция |
| 2Mg + O2 → 2MgO | Образование оксида магния |
| Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2 | Исключительная реакция для бериллия, поскольку он образует амфотерный гидроксид |
Также весьма полезна информация о том, в какой цвет окрашивают пламя атомы щёлочно-земельных металлов в соответствующих солях: для солей кальция пламя окрашивается в красный цвет, стронция в карминово-красный цвет, а для бария окраска пламени становится жёлто-зелёной.
Химические свойства гидроксидов металлов второй группы главной подгруппы
Mg(OH)2, Ca(OH)2, Ba(OH)2 и так далее – основные гидроксиды ( соответствующие оксиды – также основные), поэтому возможны реакции с кислотными оксидами и гидроксидами (в случае щёлочей возможны реакции с амфотерными гидроксидами):
Mg(OH)2 + 2HCl = MgCl2 + 2H2O
Ca(OH)2 + 2CO2 = Ca(HCO3)2
(соответствующий осадок карбоната кальция CaCO3 растворяется в избытке углекислого газа CaCO3 + CO2 + H2O = Ca(HCO3)2)
Кстати, ещё один интересный факт про CaCO3, он способен термически разлагаться (в отличие от карбонатов щелочных металлов):
CaCO3 = CaO + CO2
При написании реакций с участием гидроксидов бериллия, магния и щёлочно-земельных металлов обязательно учитываем следующие нюансы:
- Гидроксид кальция – малорастворимое вещество («М» в таблице растворимости), поэтому он выступает в качестве щёлочи в исходных веществах (реагентах) и является осадков в продуктах;
- Гидроксид магния – нерастворимое в воде вещество («Н» в таблице растворимости), поэтому в продуктах он выступает в качестве осадка:
Mg(NO3)2 + 2NaOH = Mg(OH)2 + 2NaNO3
Mg(OH)2 + FeSO4 = реакция не идёт, так как гидроксид магния нерастворим в воде
- Be(OH)2 – особый случай, в виду его амфотерности он может реагировать как с щёлочами:
Be(OH)2 + 2NaOH = Na2[Be(OH)4]
так и с кислотами:
Be(OH)2 + 2HCl = BeCl2 + 2H2O
Способы получения щёлочно-земельных металлов
Как и в случае щелочных металлов, основной способ – электролиз расплавов соответствующих солей:
CaCl2 (расплав) = Ca + Cl2
Резюме
- Металлы IIA-группы состоят из амфотерного металла бериллия, магния и щёлочно-земельных металлов;
- Характерные степени окисления металлов второй группы главной подгруппы: 0 и +2;
- Металлы IIA-группы обладают высокой восстановительной активностью.
Примеры задач на эту тему:
Задание 1. Задача №9 (из тестовой части)
Задан следующая схема превращений:
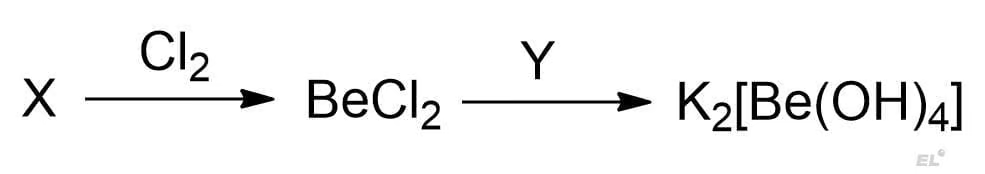
Определите неизвестные вещества X и Y:
- Be
- NaOH
- KOH
- H2O2
- KI
13
Задание 2. Задача №28 (тестовая часть)
Какой объём газа можно максимально получить при растворении 15 г кальция в избытке соляной кислоты с выходом реакции 80 %? Ответ дайте в литрах с точностью до сотых.
6,72
Задание 3. Задача №31 (открытая часть)
Кальций прореагировал с углеродом, полученное бинарное вещество растворили в соляной кислоте. К образовавшемуся раствору прилили избыток щёлочи, наблюдая образование осадка. Осадок отфильтровали, поместили в воду и пропустили через него ток углекислого газа, причём после окончания пропускания газа осадок растворился. Напишите уравнения четырёх описанных реакций.
- Ca + 2C = CaC2
- CaC2 + 2HCl = CaCl2 + C2H2
- CaCl2 + 2KOH = Ca(OH)2 + 2KCl
- Ca(OH)2 + 2CO2 = Ca(HCO3)2
Определения:
- Амфотерный гидроксид – гидроксид, проявляющий одновременно и кислотные, и основные свойства;
- Основный гидроксид – гидроксид, проявляющий основные свойства;
- Щёлочь – растворимый в воде сильный основный гидроксид.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND











