Водород
1418
Химия неметаллов открывается с водорода – элемента первой главной группы. Это самый лёгкий атом во всей вселенной, что обуславливает его огромную распространённость в космосе, межзвёздном пространстве и так далее. У атома водорода очень интересная электронная конфигурация:
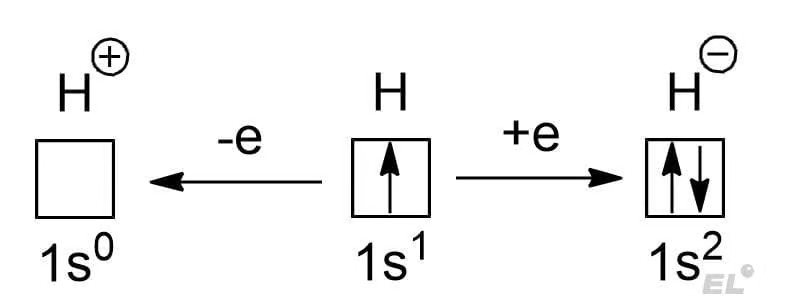
В основном состоянии он имеет единственный электрон на 1s-уровне, что открывает две возможности:
- Оторвать электрон, получив стабильную электронную конфигурацию 1s0 (катион атома водорода H+ или протон), это обуславливает характерную степень окисления +1;
- Добавить электрон, получив стабильную электронную конфигурацию 1s2 (анион атома водорода H— или гидрид-анион), это обуславливает характерную степень окисления -1.
Итак, водород может встретиться в степенях окисления -1, 0, +1. Примеры представлены в таблице:
| Степень окисления | Пример вещества |
| -1 | Гидрид натрия NaH (вещество с ионной решёткой и ионной связью между катионом натрия и гидрид-анионом) |
| 0 | Молекулярный водород H2 (двухатомная гомоядерная молекула с ковалентной неполярной связью H-H) |
| +1 | Вода H2O (вещество молекулярного строения с ковалентной полярной связью O-H) |
Для водорода также характерно наличие трёх изотопов, в ядрах атома водорода может быть:
- 0 нейтронов – этот изотоп называется протием;
- 1 нейтрон – дейтерий;
- 2 нейтрона – тритий (он радиоактивен!)
Заключительная особенность водорода – это ключевой атом в образовании водородных связей, определяющих, например, активность ферментов, нуклеиновых кислот, белков и некоторых катализаторов.
Химические свойства
- Водород в качестве окислителя: реакции с металлами
Водород более электроотрицательный чем атомы металлов, поэтому в реакции с ними образуются гидриды:
2Na + H2 → 2NaH
Ca + H2 → CaH2
Водород реагирует только с металлами первой и второй групп (главных подгрупп).
- Водород в качестве восстановителя: реакции с неметаллами и оксидами
Водород – прекрасный восстановитель за счёт своей способности повышать свою степень окисления до +1. Реагирует практически со всеми неметаллами, кроме кремния и фосфора, например:
H2 + S → H2S
N2 + 3H2 → 2NH3
Последняя реакция – обратимая каталитическая реакция синтеза аммиака, на ней основано многотоннажное промышленное производство аммиака по схеме Габера-Боша. Формула водородного соединения определяется по стандартным правилам.
Водород также может восстанавливать оксиды металлов до металлов или до оксидов металлов в более низкой степени окисления:
FeO + H2 → Fe + H2O
Fe2O3 + 3H2(избыток) → 2Fe + 3H2O
Fe2O3 + H2 → 2FeO (или Fe3O4 в недостатке H2) + H2O
Также можно восстанавливать оксиды неметаллов, классический пример, реакция каталитического получения метанола:
CO + 2H2 → CH3OH
Получение водорода
Лучший лабораторный способ – взаимодействие активного металла (но не слишком активного типа щелочных металлов, это приведёт к взрыву) с кислотой-неокислителем, например:
Zn + 2HCl → ZnCl2 + H2
В случае щелочных металлов, возможно получение водорода реакцией с водой:
2Na + 2H2O → 2NaOH + H2
Реакция очень экзотермична, поэтому проводить её стоит крайне осторожно. Также подойдут реакции амфотерных металлов или кремния с растворами щёлочей:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2
Si + 2KOH + H2O → K2SiO3 + 2H2
В качестве промышленных методов получения водорода подойдут:
- Разложение воды, при протекании через неё электрического тока: 2H2O → 2H2 + O2 (реакция электролиза);
- Окисление водой углерода (угля): C + H2O → CO + H2;
- Окисление водой метана: CH4 + H2O → CO + 3H2
Можно использовать реакции электролиза водных растворов других веществ, например солей:
Na2S + 2H2O ⟶ H2 + 2NaOH + S
Резюме:
- Водород – элемент первой группы главной подгруппы, для которого характерны степени окисления +1, 0, -1;
- Водород проявляет как окислительные свойства, так и восстановительные свойства;
- Водород – самый лёгкий атом, имеет три изотопа и является ключевым атомом в образовании водородной связи.
Примеры задач на эту тему:
Задание 1. Задача №9 (задание из первой части)
Задана следующая схема превращений:
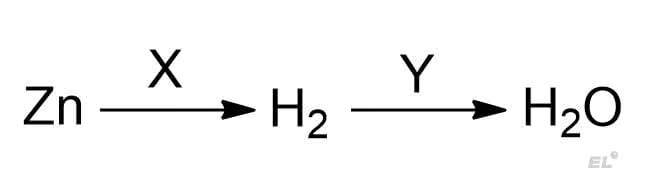
Определите, какие из указанных веществ являются веществами X и Y:
- разбавленная серная кислота
- концентрированная серная кислота
- хлор
- бромная вода
- кислород
15
Задание 2. Задача № 28 (задание из первой части)
Чему равен объём водорода (при н.у.), который выделился при взаимодействии 65 г цинка с избытком разбавленной серной кислоты?
22,4 л
Задание 3. Задача №31 (задание из второй части)
Металлический натрий оставили в атмосфере водорода, причём водород был взят в недостатке. Полученный твёрдый остаток растворили в воде. Образованный раствор прилили к раствору нитрата магния, наблюдая образование осадка. Напишите молекулярные уравнения четырёх описанных реакций.
- 2Na + H2 ⟶ 2NaH
- 2Na + 2H2O ⟶ 2NaOH + H2
- NaH + H2O ⟶ NaOH + H2
- Mg(NO3)2 + 2NaOH ⟶ Mg(OH)2 + 2NaNO3
Определения:
- Атом водорода – самый лёгкий, потому что имеет наименьшую молярную массу 1 г/моль.
- Изотопы – атомы, имеющие в своём ядре одинаковое число протонов, но разное число нейтронов.
- Радиоактивность – явление выделения высокоэнергетических частиц (например, альфа-частиц или света) при распаде нестабильных ядер.
- Водородная связь – химическая связь, возникающая между электроотрицательным атомом (N, O, F) и водородом, связанным напрямую с электроотрицательным атомом (N, O, F).
- С кремнием и фосфором реакция не идёт, так как они обладают схожей с водородом электроотрицательностью.
- Для расчёта формулы водородного соединения воспользуемся формулой расчёта наинизшей степени окисления: номер группы – 8, например, для серы получаем 6 – 8 = -2, откуда H2S.
- Кислоты-неокислители – кислоты, которые могут ярко проявлять окислительные свойства только за счёт H+1 в своём составе.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND











