Обратная связь
Была ли эта статья тебе полезной?
Всё ли было понятно? Оставляй обратную связь, мы это ценим
Не трать свое время на поиски нужной инфы, пользуйся нашим учебником.
Самая используемая формула молекулярки — уравнение Менделеева-Клапейрона, которое связывает три основных макроскопических параметров, описывающих идеальный газ, — давление, объем и температуру. Можно экспериментировать с газом и получать частные случаи данной формулы. Рассмотрим, в каких термодинамических процессах может участвовать газ.
Изопроцесс — процесс, при котором один из параметров (давление газа p, объем газа V или температура газа T) остается постоянным, при этом масса газа в процессе также неизменна.
Всего разделяют три изопроцесса:
Рассмотрим каждый процесс отдельно.
1. Изотермический процесс — процесс изменения состояния газа определенной массы при постоянной температуре
T = const, m = const
Запишем уравнение Менделеева-Клапейрона:
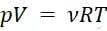
Так как количество вещества , газовая постоянная R и температура T неизменны, то произведение давления и объема не изменяются.
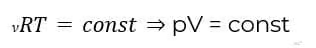
Таким образом, для изотермического процесса справедлив закон Бойля-Мариотта:
pV = const
или
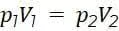
Графиком изменения состояния газа в изотермическом процессе является изотерма:
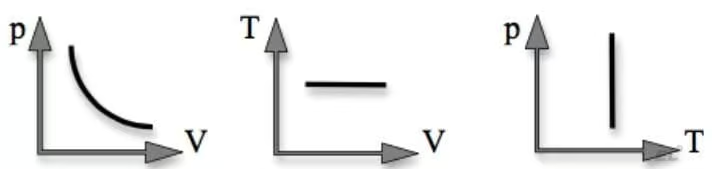
2. Изохорный процесс — процесс изменения состояния газа определенной массы при постоянном объеме
V = const, m = const
Для изохорного процесса справедлив закон Шарля:
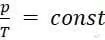
или
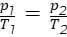
Графиком изменения состояния газа в изохорном процессе является изохора:
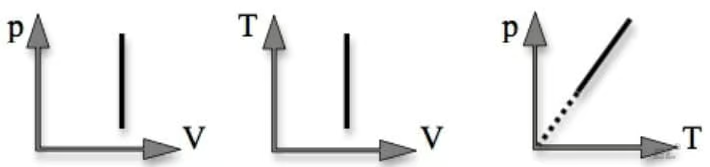

3. Изобарный процесс — процесс изменения состояния газа определенной массы при постоянном давлении
p = const, m = const
Для изобарного процесса справедлив закон Гей-Люссака:
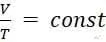
или
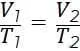
Графиком изменения состояния газа в изобарном процессе является изобара:
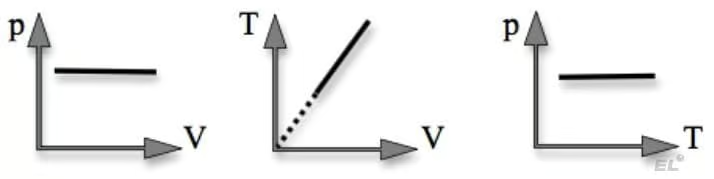
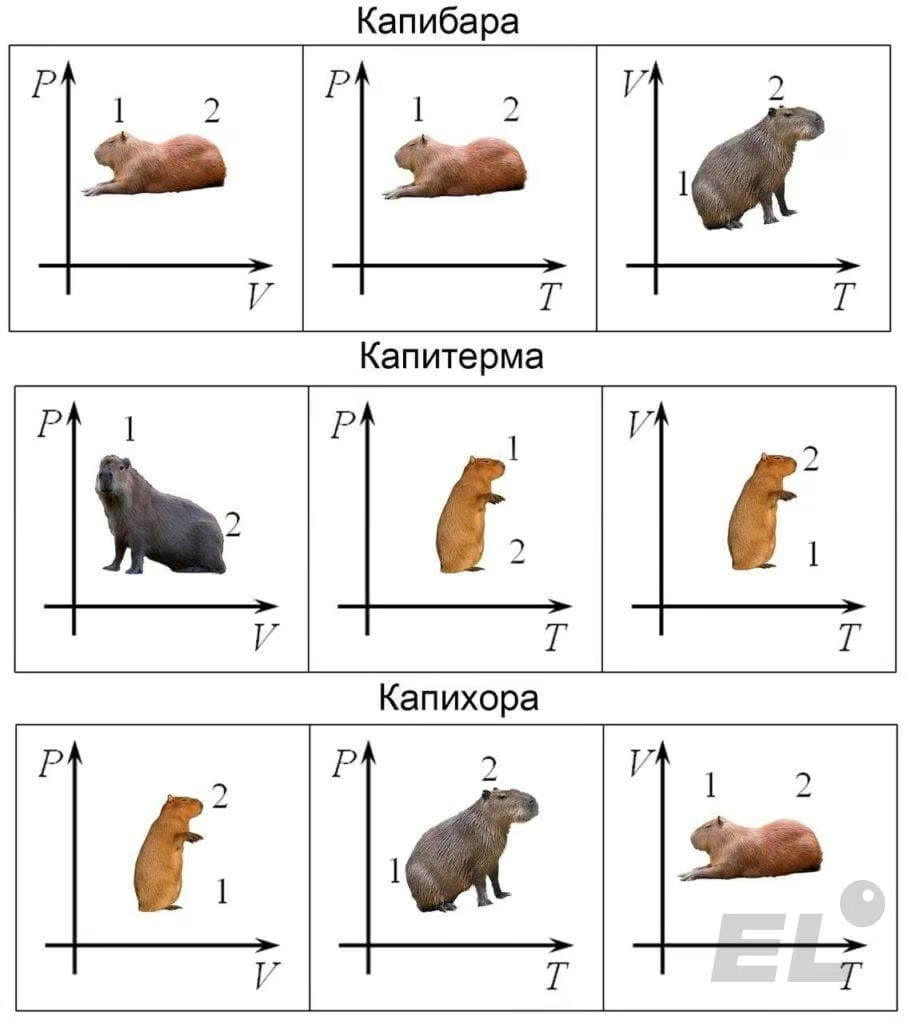
В общем случае, если масса газа постоянна, но остальные параметры меняются, то из уравнения Менделеева-Клапейрона следует выражение:
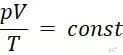
или
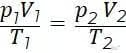
Работа газа
Рассмотрим газ, который находится в сосуде под подвижным поршнем. В какой-то момент газ начинает расширяться — увеличивать занимаемый им объем. В таком случае говорят, что газ совершает положительную работу — 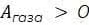
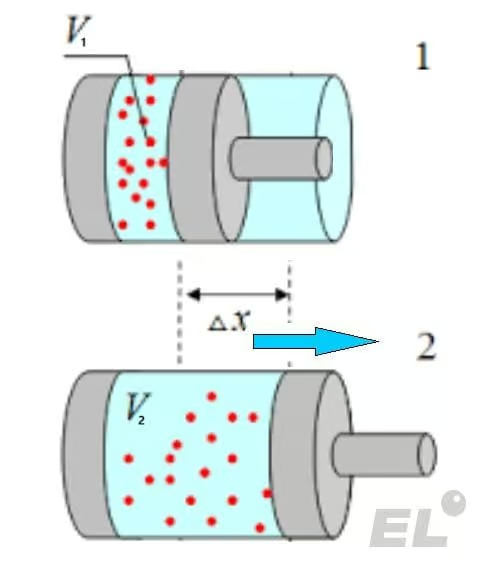
Если же газ сжимают — объем газа уменьшается, то, говорят, что внешние силы совершают положительную работу над газом — 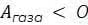
Как же вычислить работу газа? В общем случае работа газа равна площади под графиком в pV-осях:
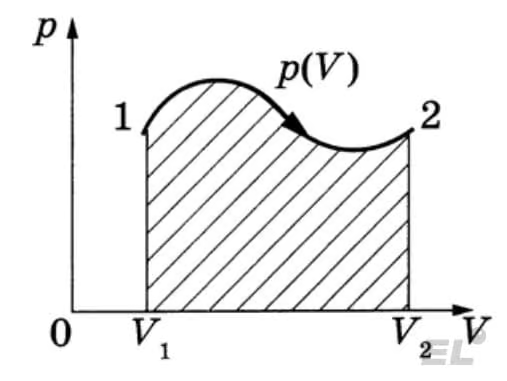
В изохорном процессе работа газа равна нулю, так как объем в данном процессе не изменяется. В изобарном процессе площадь под графиком процесса равна площади прямоугольника, поэтому работу газа можно найти как
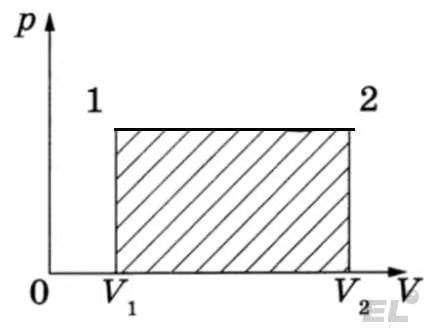
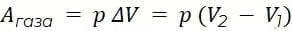
Для изотермического процесса тоже существует формула для нахождения работы газа, но она, как правило, не рассматривается в школьном курсе физики и не встречается на ЕГЭ.

Первое начало термодинамики
Все встречались с законом сохранения энергии в механике, в термодинамике частный случай ЗСЭ называется первым началом (или законом) термодинамики. Пусть газ получает количество теплоты Q от окружающего мира (например, зимой окружающий воздух дома нагревается за счет батареи), что же тогда происходит с газом? Он тратит это количество теплоты на изменение своей внутренней энергии 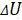 и совершает работу
и совершает работу 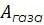 .
.

Первое начало термодинамики записывается в виде:
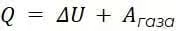
Где изменение внутренней энергии газа определяется изменение температуры:
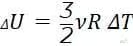
Первый закон термодинамики выглядит очень просто, но охватывает множество частных случаев!
1. Q > 0, если система получает тепло, и Q < 0, если отдает. Q = 0 если теплообмена с окружающей средой нет (такой процесс называется адиабатическим (не является изопроцессом)).
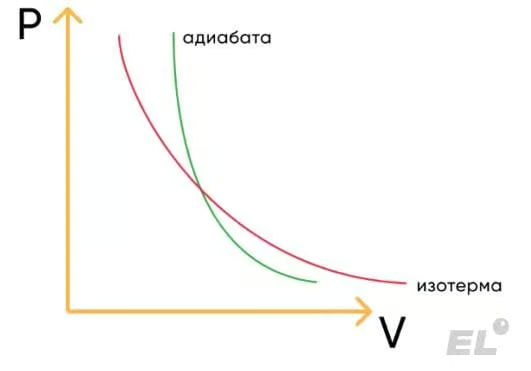
График адиабатного процесса схож с изотермическим:
2. 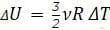 , поэтому
, поэтому 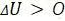 , если
, если 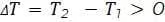 , то есть температура газа повышается, и
, то есть температура газа повышается, и 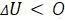 , если
, если 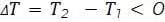 , то есть температура газа понижается. Отдельно стоит отметить изотермический процесс — процесс, в котором масса газа и температура не изменяются. В таком случае
, то есть температура газа понижается. Отдельно стоит отметить изотермический процесс — процесс, в котором масса газа и температура не изменяются. В таком случае 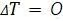 , и как следствие,
, и как следствие, 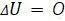
3. 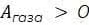 , если газ совершает работу (объем, занимаемый газом, увеличивается), и
, если газ совершает работу (объем, занимаемый газом, увеличивается), и 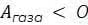 , если работа совершается над газом (объем, занимаемый газом уменьшается). В изохорном процессе (процесс, в котором масса газа и его объем неизменны)
, если работа совершается над газом (объем, занимаемый газом уменьшается). В изохорном процессе (процесс, в котором масса газа и его объем неизменны) 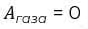 вследствие постоянного объема газа.
вследствие постоянного объема газа.
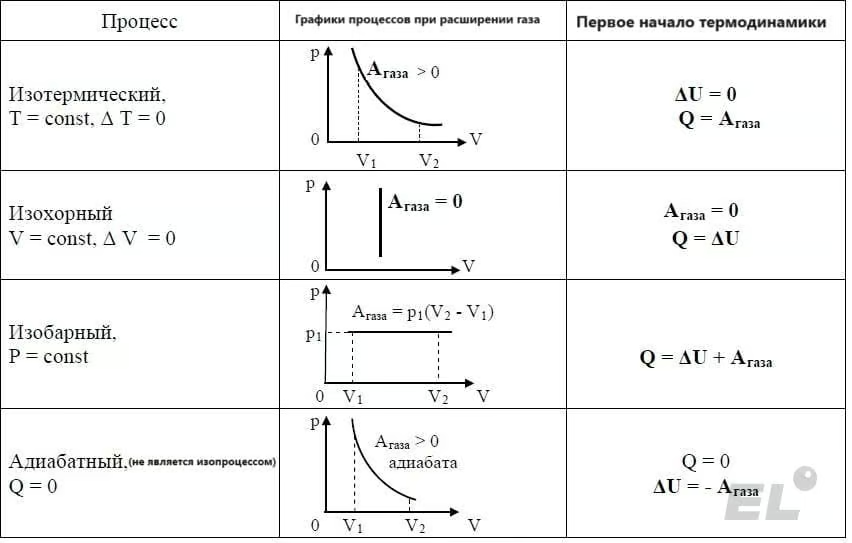
Резюме:
Задание 1. Задание № 7 (тестовая часть)
На рисунке представлен график зависимости объема идеального газа от его температуры в некотором процессе. В состоянии 1 давление газа было равно нормальному атмосферному давлению. Какое давление соответствует состоянию 2, если масса газа остается неизменной? Приведите ответ в кПа.
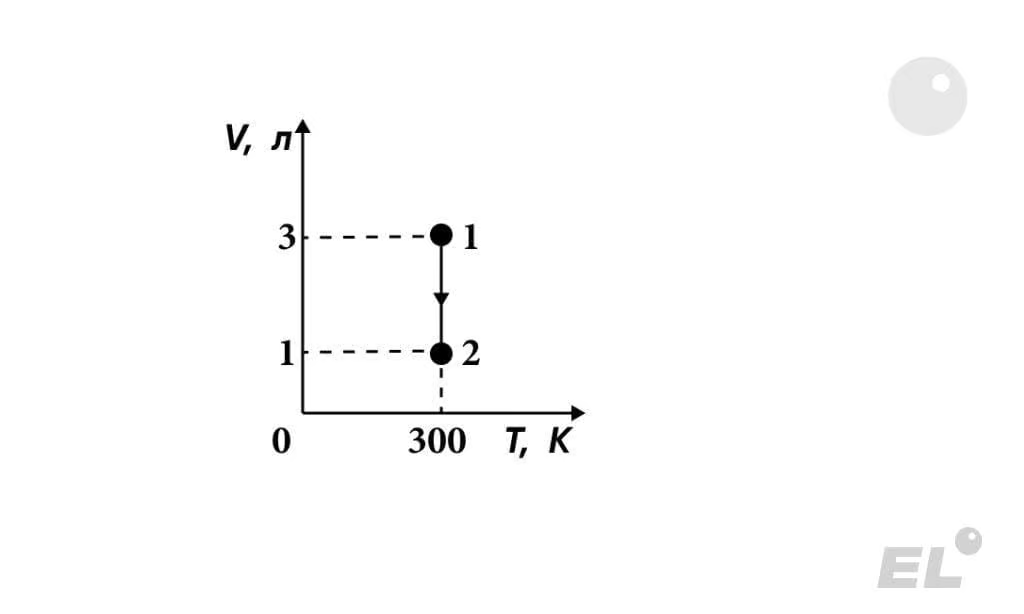
300
Источник: Сборник Демидова 30 вариантов 2023
Задание 2. Задание № 9 (тестовая часть)
Зависимость температуры 1 моль одноатомного идеального газа от давления показана на рисунке. Выберите из предложенных утверждений все, которые верно отражают результаты этого эксперимента.
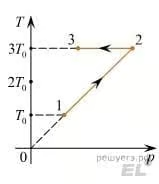
25
Источник: Демонстрационная версия ЕГЭ — 2019 по физике
Задание 3. Задание № 21 (вторая часть)
На рисунке изображены графики двух процессов, проведённых с идеальным газом при одном и том же давлении. Графики процессов представлены на рисунке. Почему изобара I лежит выше изобары II? Ответ поясните, указав, какие физические закономерности Вы использовали для объяснения.
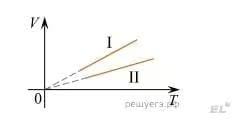
Источник: ЕГЭ по физике 2013, основная волна
Была ли эта статья тебе полезной?
Всё ли было понятно? Оставляй обратную связь, мы это ценим
Тогда заполняй все поля и жди сообщения от нашего менеджера из отдела заботы



Обязательно заполните все поля, иначе мы не сможем точно подобрать подготовку