Переходные элементы
1457
Перейдём к рассмотрению некоторых переходных металлов: хрому, марганцу, железу, меди, серебру, платине, золоту и ртути. Начнём с общей характеристики:
| Металл | Физические свойства при н.у. | Конфигурация валентных электронов | Характерные степени окисления |
| Cr | Серебристый металл | 3d5 4s1 | 0, +2, +3, +6 |
| Mn | Серебристый металл | 3d5 4s2 | 0, +2, +4, +7 |
| Fe | Серебристый металл | 3d6 4s2 | 0, +2, +3, +6 |
| Cu | Красноватый металл | 3d10 4s1 | 0, +1, +2 |
| Ag | Серебристый металл | 4d10 5s1 | 0, +1 |
| Hg | Жидкий металл | 5d10 6s2 | 0, +1, +2 |
| Pt | Серебристый металл | 5d9 6s1 | 0, +2, +4 |
| Au | Золотистый металл | 5d10 6s1 | 0, +1, +3 |
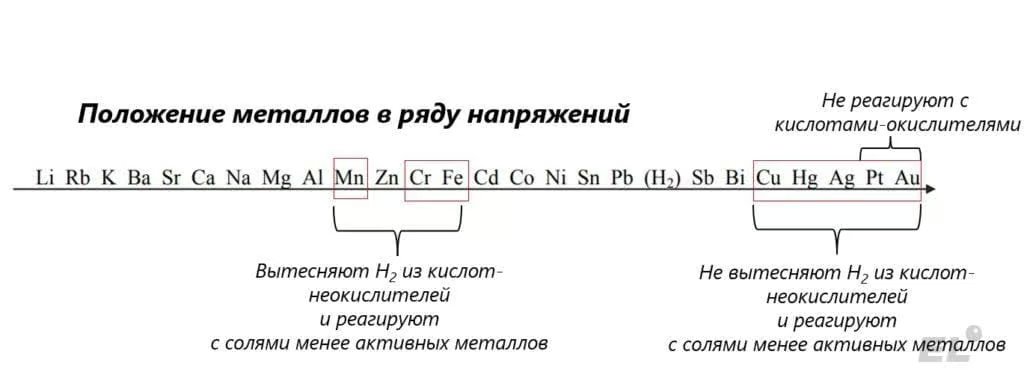
В случае хрома, марганца и железа, как видно, наблюдается, широкое разнообразие в степенях окисления, что связано с неполностью заполненным d-подуровнем в сравнении с медью, серебром и ртутью. Перечислим основные химические реакции, в которые вступают данные простые вещества:
| Реакция | Примеры реакций |
| Сжигание в O2 | 4Cr + 3O2 = 2Cr2O3 3Fe + 2O2 (недостаток) = Fe3O4 (железо в степенях окисления +2 и +3) 4Fe + 3O2 (избыток) = 2Fe2O3 2Cu + O2 = 2CuO 2Hg + O2 = 2HgO 2Ag + 2H2S + O2 = 2Ag2S + 2H2O (Ag2S – чёрный, поэтому в ходе этой реакции серебро «чернеет» |
| Сжигание в Cl2 | 2Fe + 3Cl2 = 2FeCl3 2Cr + 3Cl2 = 2CrCl3 Cu + Cl2 = CuCl2 Hg + Cl2 = HgCl2 2Ag + Cl2 = 2AgCl |
| Реакция с I2 | Fe + I2 = FeI2 (FeI3 разлагается на FeI2 и I2) 2Cu + I2 = 2CuI (CuI2 разлагается на CuI и I2, пример подобной реакции: 2CuSO4 + 4KI = 2CuI + I2 + 2K2SO4) |
| Реакция с S | Fe + S = FeS (Fe2S3 разлагается на FeS и S, пример подобной реакции: 2FeCl3 + 3Na2S = 2FeS + S + 6NaCl) Cu + S = CuS |
| Реакция с кислотами | Fe + 6HNO3(конц.) = Fe(NO3)3 + 3NO2 + 3H2O (с концентрированными HNO3, H2SO4 железо и хрома не реагируют при обычных условиях в виду явления пассивации) Cr+ 2HCl = CrCl2 + H2 Cu + HCl = реакция не идёт, так как медь в ряду напряжений стоит после H Ag + HCl = реакция не идёт, так как медь в ряду напряжений стоит после H Au + H2SO4 (конц.) = реакция не идёт, так как золото, как и платина, является благородным металлом |
В случае железа, меди и хрома можно заметить некоторые закономерности в зависимости от того какой окислитель (слабый или сильный) берём:
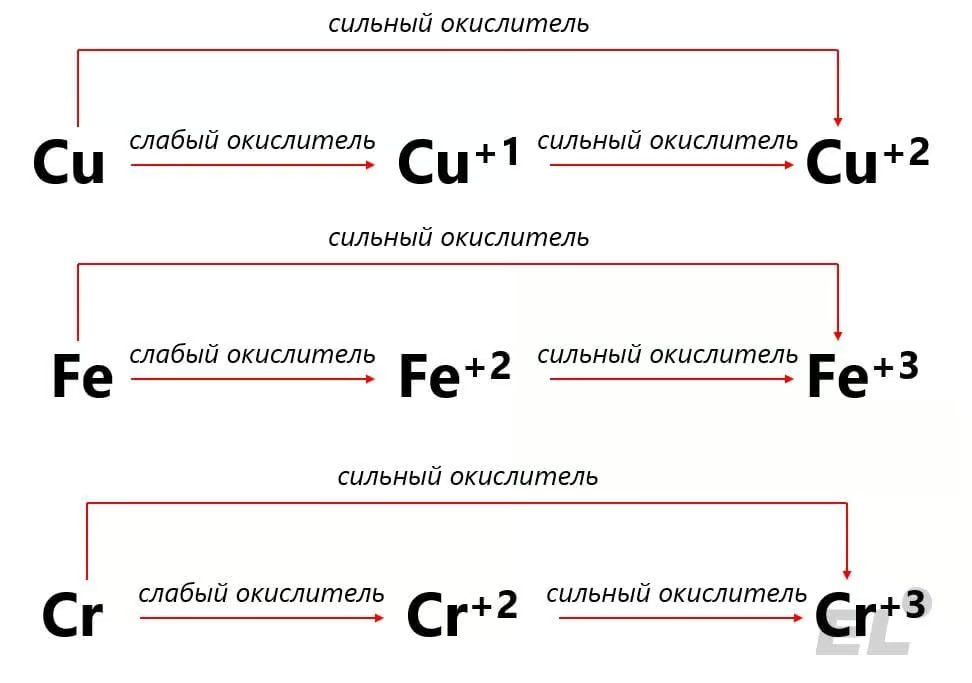
Можем просуммировать:
- Соединения Cu+1 проявляют восстановительные свойства, а Cu+2 окислительные свойства (соответствующие гидроксиды CuOH, Cu(OH)2 и оксиды Cu2O, CuOH проявляют основные свойства, причём CuOH неустойчив и распадается на кирпично-красный Cu2O и воду);
- Соединения Fe+2 проявляют восстановительные свойства, а Fe+3 окислительные (восстановительные свойства также могут проявляться, путём окисления до степени окисления +6) свойства (FeO и Fe(OH)2 проявляют основные свойства, а Fe2O3, Fe(OH)3 амфотерные свойства);
- Соединения Cr+2 проявляют восстановительные свойства, а Cr+3 окислительные и восстановительные свойства (CrO, Cr(OH)2 проявляют основные свойства, а Cr2O3, Cr(OH)3 амфотерные свойства), в свою очередь, соединения Cr+6 являются сильными окислителями (CrO3, H2CrO4 и H2Cr2O7 проявляют кислотные свойства);
- Соединения Mn+2 проявляют восстановительные свойства, Mn+4 и окислительные, и восстановительные свойства, Mn+6 и окислительные, и восстановительные свойства, а Mn+7 сильные окислительные свойства (MnO, Mn(OH)2 – основные свойства, MnO2 – амфотерные свойства, MnO3, H2MnO4 – кислотные свойства, Mn2O7, HMnO4 – кислотные свойства).
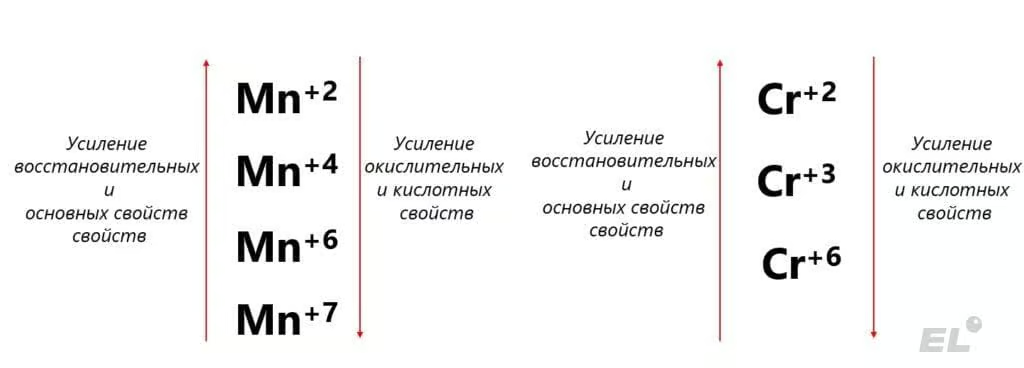
Наконец, приведём характерные окислительно-восстановительные реакции и реакции ионного обмена переходных элементов в разных степенях окисления:
| Элемент | Схема реакции |
| Fe+2 | 
|
| Fe+3 | 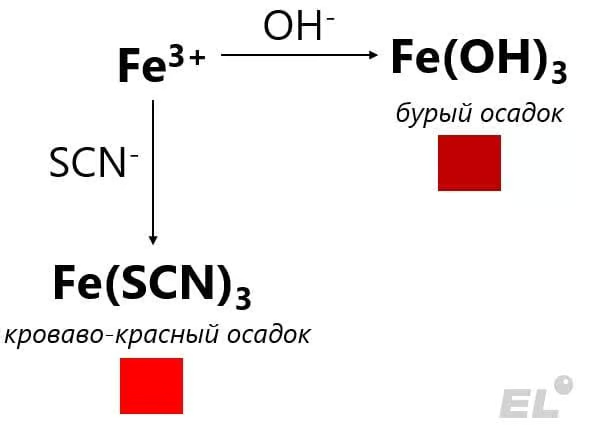
|
| Cu+2 | 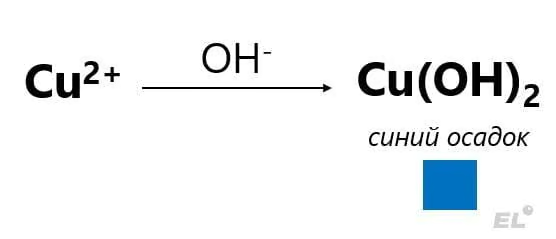
|
| Ag+1 | 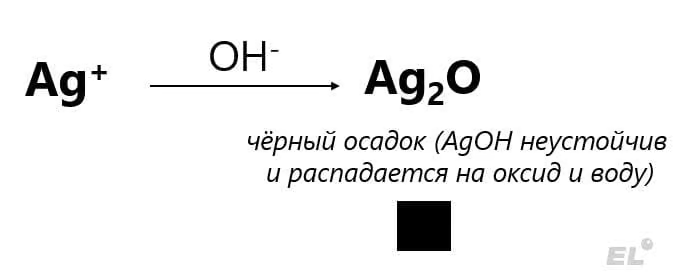
|
| Mn+4 | 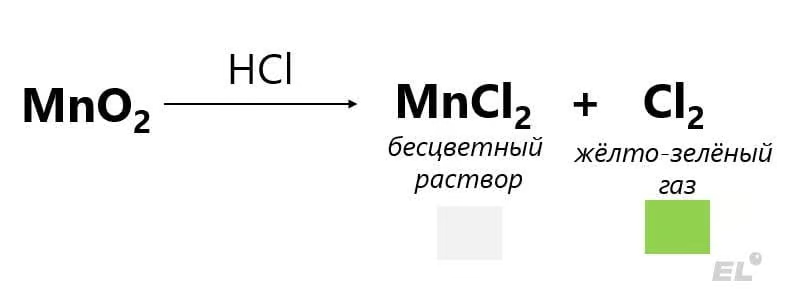
|
| Mn+7 | 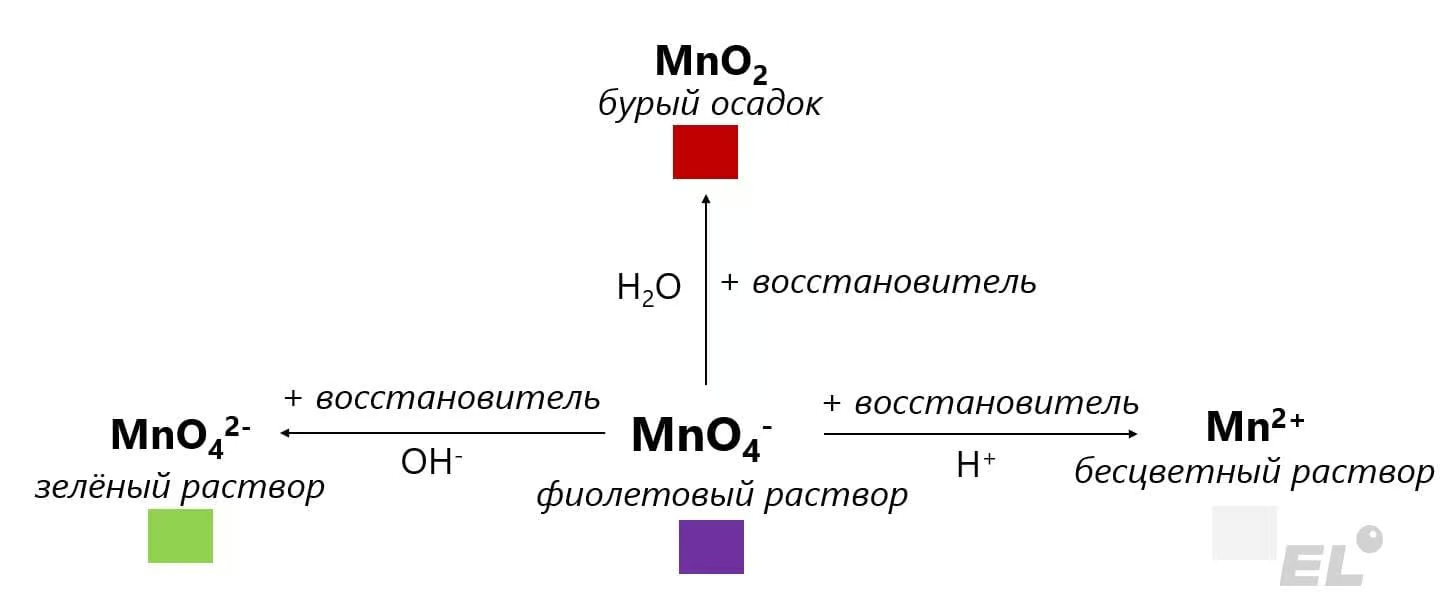
|
| Cr+6 | 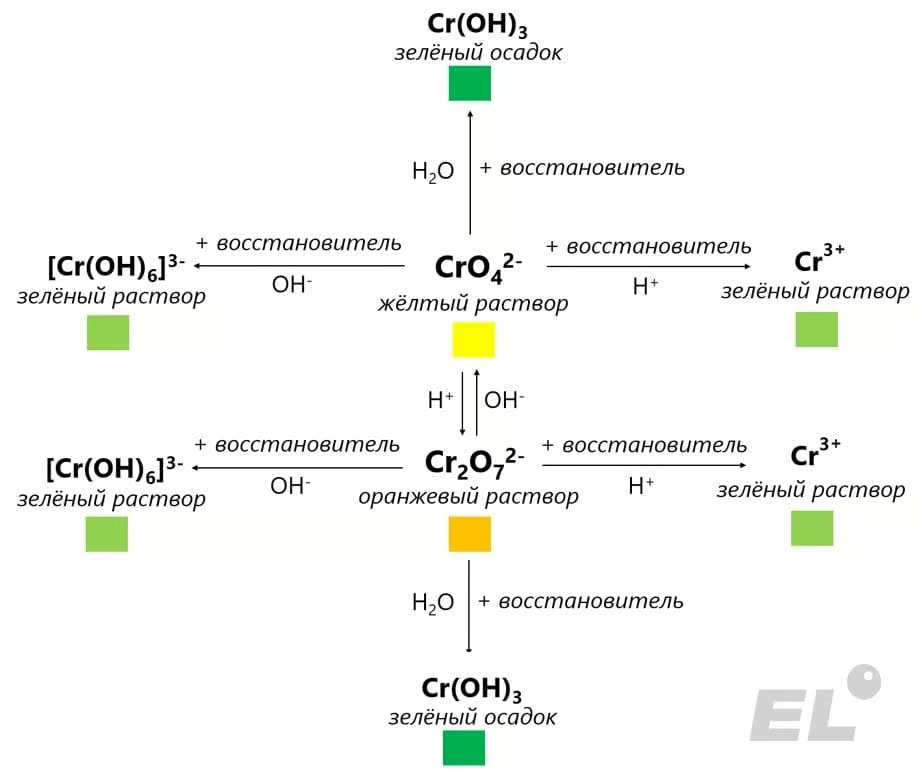
|
Резюме:
- Для марганца характерны степени окисления: 0, +4, +6 и +7.
- Для хрома характерны степени окисления: 0, +2, +3 и +6.
- Наиболее характерные степени окисления железа: 0, +2 и +3.
- Медь и ртуть проявляют степени окисления от 0 до +2.
- Для серебра наиболее устойчивыми степенями окисления являются 0 и +1.
- Золото и платина являются благородными металлами.
Примеры задач на эту тему:
Задание 1. Задача №1 (первая часть)
1) Ca 2) Sr 3) Cu 4) Cr 5) S
Из указанных в ряду элементов, выберите два элемента, которые имеют единственный внешний электрон в основном состоянии.
3 4
Задание 2. Задача №3 (первая часть)
1) Mn 2) Se 3) N 4) Cr 5) P
Из указанных в ряду элементов, выберите два элемента, которые проявляют максимальную степень окисления, равную +6.
2 4
Задание 2. Задача №31 (вторая часть)
Навеску железа разделили на две части. Первую часть сожгли в хлоре. Полученное бинарное вещество растворили в воде, а затем прилил избыток щёлочи, наблюдая выпадение бурого осадка. Вторую часть навески растворили в соляной кислоте, полученный раствор обработали щёлочью. Напишите уравнения четырёх описанных реакций.
- 2Fe + 3Cl2 = 2FeCl3
- FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl
- Fe + 2HCl = FeCl2 + H2
- FeCl2 + 2NaOH = Fe(OH)2 + 2NaCl
Определения:
- Переходные металлы – металлы побочных подгрупп главных групп, обладающих валентными d-электронами.
- Пассивация – явление покрытия труднорастворимой оксидной плёнкой поверхности таких металлов как Fe, Ni, Cr и Al при действии на них концентрированными HNO3 и H2SO4 при комнатной температуре.
- Благородные металлы – инертные металлы, не растворяющиеся в кислотах-окислителях.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND











