Строение атомов
1089
Наш мир состоит из маленьких «кирпичиков» – атомов, которые образуют разнообразные вещества. Атом включает в свой состав положительно-заряженное ядро и отрицательно-заряженные электроны:
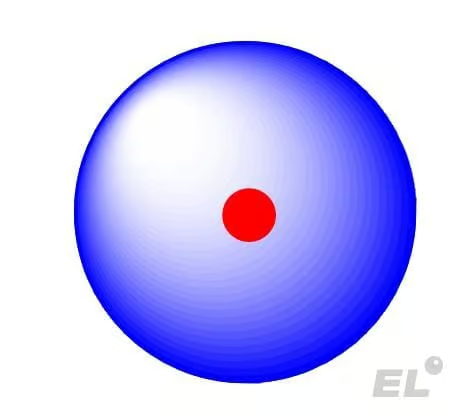
Наглядная модель атома: в центре находится маленькое ядро (красный шарик), в котором сконцентрирована практически вся масса атома (масса ядра в ~2000 раз больше массы элетрона), а вокруг него размазаны электроны в виде синего облака.
Ядро, в свою очередь, состоит из нуклонов: положительно-заряженных протонов и нейтральных нейтронов. Причём поскольку атом нейтральная частица, то число протонов равно числу электронов.
Итак, перейдём к более конкретному описанию атомов химических элементов. Каждый химический элемент характеризуется:
- Числом протонов в ядре (порядковый номер) – это и определяет химический элемент;
- Атомной массой (сумма масс электронов, протонов и нейтронов, образующих атом), причём поскольку протоны и нейтроны значительно тяжелее электронов по массе, то основной вклад в массу вносят именно нуклоны;
- Числом электронов – их число равно числу протонов (порядковому номеру) элемента.
Все данные свойства атомов химических элементов удобно собраны в периодической таблице Менделеева:
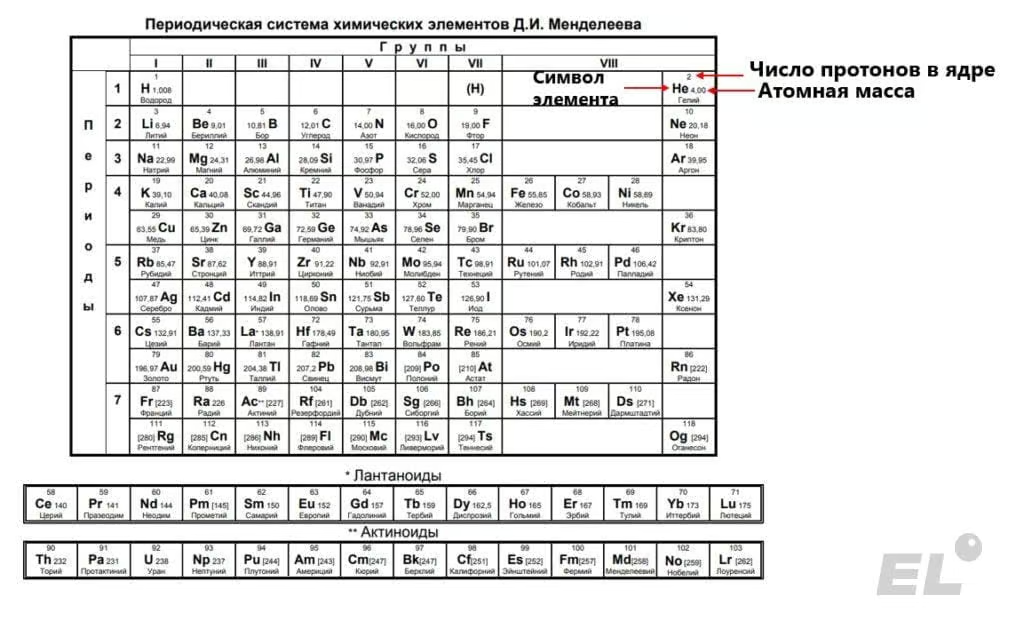
Таблица Менделеева (вид как на ЕГЭ). Её особенности показаны на примере гелия.
Пример: возьмём атом гелия He. Его порядковый номер равен двум, то есть в его ядре находится 2 протона, и, как следствие, два электрона есть в данном атоме. Найдём число нейтронов в ядре атома гелия как разность между атомной массой и числом протонов: 4 – 2 = 2 нейтрона.
Состояние электронов в атомах
Перейдём к описанию электронов в атомах. Для описания состояния электронов в атоме необходимо задать:
- Орбиталь – по сути, место вокруг ядра атома, в котором «живёт» данный электрон. Орбитали бывают разной формы: s, p, d-орбитали:
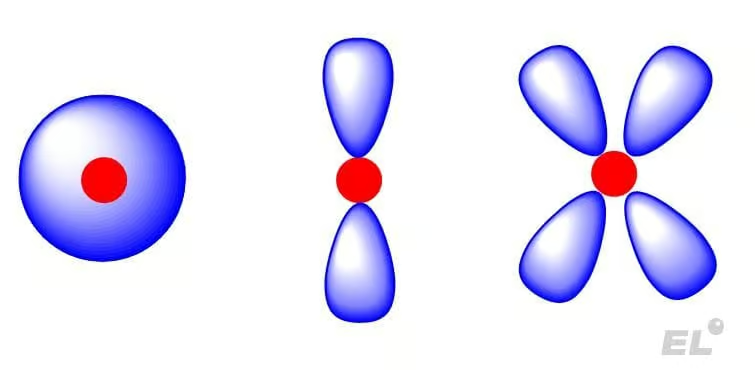
Формы s, p, d-орбиталей (слева направо). Красным шариком показано ядро атома, синий цвет показывает область пространства, где может быть электрон.
- Направление спина электрона – стрелочка вверх или стрелочка вниз. Обычно орбитали показывают в форме квадратика (клеточки), например, орбиталь, занятая парой электронов выглядит так:

Орбиталь, заполненная двумя электронами
Правила составления электронных конфигураций
При составлении электронных конфигураций необходимо руководствоваться некоторыми правилами. Пройдёмся по ним:
- Принцип Паули: на одной орбитали могут находиться максимально два электрона с разным направлением спина, то есть направление стрелочек в клеточке всегда противоположно:

Принцип Паули
- Правило Хунда: электроны заселяют орбитали таким образом, чтобы обеспечить максимально число электронов со стрелочкой вверх (максимальным спином, направленным вверх), например:
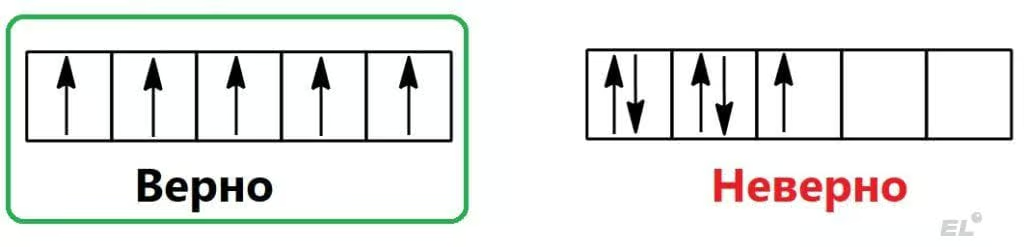
Правило Хунда
- Правило Клечковского: орбитали заполняются электронами в строго определённом порядке. В начале заполняются орбитали с наименьшей энергии, затем с более высокой энергией и так далее: электроны в атоме стремятся иметь наименьшую возможную энергию. Порядок заполнения орбиталей показан зелёными стрелками:
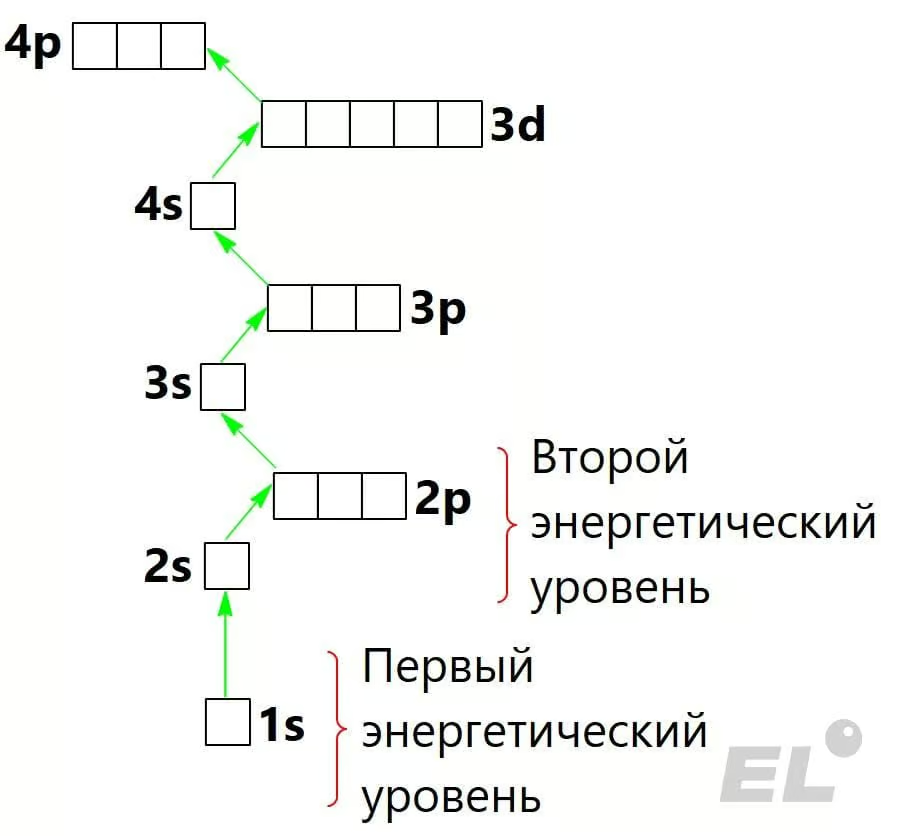
Порядок заполнения орбиталей
Очень важно понимать следующие утверждения:
- Первый энергетический уровень включает в себя только 1s-орбиталь (циферка перед орбиталью – номер энергетического уровня);
- Второй энергетический уровень включает в себя два подуровня: одна 2s-орбиталь и три 2p-орбитали;
- Число s-орбиталей: 1 (одна клеточка на любом энергетическом уровне), число p-орбиталей: 3 (три клеточки, начиная со второго энергетического уровня), число d-орбиталей: 5 (пять клеточек, начиная с третьего энергетического уровня).
В заполнении электронных конфигураций может сильно помочь таблица Менделеева:
- Номер периода определяет число энергетических уровней в атоме;
- Номер группы определяет число валентных электронов в атоме.
Пример: возьмём атом фтора. Он находится во втором периоде, то есть имеем два энергетических уровня для заполнения: 1s 2s 2p. Порядковый номер фтора равен 9, то есть необходимо раскидать по этим орбиталям 9 электронов:
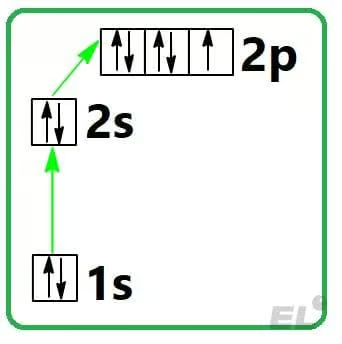
Электронная конфигурация атома фтора
Обычно это записывают, указывая верхним индексом сколько электронов занимает соответствующий подуровень 1s2 2s2 2p5. Поскольку последний заполненный подуровень 2p, то фтор считается p-элементом. В данном случае:
- 2s2 2p5 – валентные (= внешние только для s и p-элементов) электроны, так как у нас всего два энергетических уровня
- Фтор в седьмой группе и имеет 7 валентных электронов: 5 + 2 = 7 – всё верно
Особенности электронного строения атомов d-элементов
Для того, чтобы понять какие сложности возникают с атомами d-элементов, рассмотрим два поучительных примера:
- Атом титана: он находится в четвёртом периоде (= 4 энергетических уровня), в четвёртой группе (= 4 валентных электрона) и имеет номер 22 (= 22 электрона в атоме всего). Заполняем первые 18 электронов 1s2 2s2 2p6 3s2 3p6. Дальше заполняется не 3d-подуровень, а 4s, поэтому 1s2 2s2 2p6 3s2 3p6 4s2 3d2. Как раз-таки 4s2 3d2 мы и считаем валентными электронами у атома титана – он d-элемент. Поскольку титан является d-элементов, то возникает разница между внешними и валентными электронами. Внешние только 4s2 в то время как валентные 4s2 3d2.
- Атом меди: аналогично заполняем 1s2 2s2 2p6 3s2 3p6 4s2 3d9. Тут возникает нюанс: выгодно сделать d-уровень полностью заполненным (или наполовину заполненным), поэтому один s-электрон перейдёт на d-подуровень и будет 1s2 2s2 2p6 3s2 3p6 4s1 3d10. Это явление называется электронным провалом. Аналогичный эффект, например, наблюдается для хрома 1s2 2s2 2p6 3s2 3p6 4s1 3d5 вместо 1s2 2s2 2p6 3s2 3p6 4s2 3d4.
Основное и возбуждённое состояния атомов
Все правила, которые были сформулированы выше относятся именно к основным состояниям атомов. Например, у атома серы электронная конфигурация основного состояния 1s2 2s2 2p6 3s2 3p4 (третий период – 3 энергетических уровня, шестая группа – 6 валентных электронов). Мы можем, например, перенести один из электронов с 3p-подуровня на 3d: 1s2 2s2 2p6 3s2 3p3 3d1 – такое состояние будет иметь более высокую энергию и называется возбуждённым.
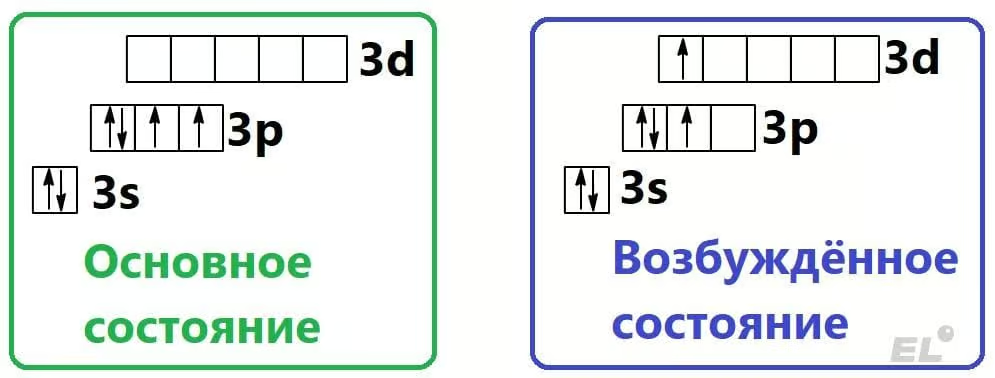
Основное состояние 1s2 2s2 2p6 3s2 3p4 и возбуждённое состояние 1s2 2s2 2p6 3s2 3p3 3d1 атома серы
Построение электронных конфигураций заряженных частиц: катионов и анионов
Возьмём атом и заберём у него один или несколько электронов, он станет положительно-заряженной частицей – катионом. Если наоборот дать атому несколько электронов, то он станет отрицательно-заряженной частицей – анионом. Как строить конфигурации катионов и анионов, зная конфигурацию исходного атома? Очень просто, используем следующие правила:
- Электронная конфигурация натрия 1s2 2s2 2p6 3s1. Тогда, чтобы получить конфигурацию иона Na+ убираем один электрон с последнего подуровня 3s: 1s2 2s2 2p6 3s0
- Электронная конфигурация фосфора 1s2 2s2 2p6 3s2 3p3. Чтобы составить конфигурацию аниона P3- добавляем 3 электрона к последнему подуровню 3p: 1s2 2s2 2p6 3s2 3p6
Резюме
- Атомы состоят из положительно-заряженных ядер и отрицательно-заряженных электронов;
- Электроны заполняют орбитали согласно правилам Паули, Хунда и Клечковского;
При составлении электронных конфигураций d-элементов стоит помнить про различие внешних и валентных электронов, а также не забывать про явление электронного провала.
Примеры задач на эту тему:
Задание 1. Задача №1 (первая часть)
Для решения задания используйте следующий ряд химических элементов:
1) N 2) Na 3) Cr 4) O 5) C
Выберите два элемента, которые имеют ровно один внешний электрон в основном состоянии
2 3
Задание 2. Задача №3 (первая часть)
Для решения задания используйте следующий ряд химических элементов:
1) N 2) Li 3) F 4) Se 5) C
Выберите два элемента, которые проявляют максимальную валентность, равную IV.
14
Задание 3. Задача №28 (первая часть)
При взаимодействии 60 г Na2SO3 с соляной кислотой выделилось 8,96 л (н.у.) диоксида серы. Вычислите массовую долю (в %) примесей в указанном сульфите. (Запишите число с точностью до целых в процентах)
16
Определения:
- Химический элемент – по сути, совокупность атомов, обладающих определённым зарядом ядер (одинаковым числом протонов в ядре).
- Орбиталь – её можно ассоциировать с областью пространства вокруг ядра атома, в которой с определённой вероятностью может быть электрон.
- Спин электрона – вектор момента импульса, непосредственно связанный с электроном, который может быть направлен либо вдоль определённой оси, либо против неё.
- Электронная конфигурация атома – запись в форме 1s22s2…, показывающая какие орбитали заселены электронами и сколько электронов (верхний индекс) находится на данных орбиталях.
- Электронный провал (проскок) – явление, которое заключается в устойчивости полузаполненных или полностью заполненных d-оболочек атомов.
- Основное состояние атома – состояние атома с наименьшей энергией, то есть имеется в виду такая электронная конфигурация (заполнение орбиталей), которая соответствует наименьшей возможной энергии.
- Возбуждённое состояние атома – состояние атома, которое обладает большей энергией, чем его основное состояние.

Хочешь начать готовиться, но остались вопросы?
Заполни форму, и мы подробно объясним, как устроена подготовка к ЕГЭ и ОГЭ в ЕГЭLAND











